PROTOZOOS
Los protozoos son organismos unicelulares. Viven en una gran variedad de hábitats húmedos, incluyendo el agua dulce, ambientes marinos y el suelo. Ellos se han dividido tradicionalmente sobre la base de sus medios de locomoción: flagelados, rizópodos, esporozoos, y ciliados. Varias especies de cada uno de estos grupos protozoario están asociadas con enfermedades humanas. Los cuatro grupos son patógenos intestinales, pero sólo los flagelados y esporozoos son clasificadas aun mas como protozoos sanguíneas y tisulares*.
|
RIZÓPODOS
Entamoeba histolytica Naegeria fowleri Acanthamoeba spp Balamuthia mandrillaris FLAGELADOS Giardia lamblia Trichomonas vaginalis Trypanosoma spp* Leishmania spp* |
CILIADOS
Balantidium coli ESPOROZOOS Cryptosporidium parvum Cyclospora cayetanensis Isospora belli Plasmodium spp* Toxoplasma gondii* |
RIZÓPODOS
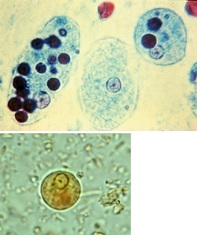 Trofozoito (arriba)
Quiste (abajo)
Trofozoito (arriba)
Quiste (abajo)
AMEBIASIS (Amebiasis intestinal, Amebiasis hepatica)
Entamoeba histolytica
Philum: Amoebozoa
Clase: Archamoebae
Orden: Entamoebida
Género y Especie: Entamoeba histolytica
EPIDEMIOLOGÍA
0.5 a 50% de la población mundial alberga parásitos E. histolytica con las tasas más altas de infección en los países subdesarrollados. La infección se asocia con la falta de higiene. Los seres humanos son el principal huésped.
MORFOLOGÍA
Trofozoíto: Forma patogena. Tiene un aspecto ameboide y es por lo general 20 a 50 micrómetros de diámetro. El organismo tiene un único núcleo con un pequeño cariosoma central. El endoplasma granular fino puede contener eritrocitos ingeridos. La cromatina nuclear se distribuye uniformemente por la periferia del núcleo.
Quiste: Forma infectante. Contiene de 1 a 4 núcleos. Son de forma redondeada, refringente con una membrana claramente demarcada. En el citoplasma se pueden ver cuerpos cromatidales.
CICLO DE VIDA
La infección se produce por la ingestión de quistes en los alimentos o las manos con contaminación fecal. El quiste es resistente al medio gástrico y pasa a la intestino delgado, donde eclosiona. El metaquiste se divide en cuatro y luego ocho amebas que se mueven al intestino grueso. La mayoría de los organismos se hacen pasar fuera del cuerpo con las heces, pero, si las condiciones son propicias los trofozoítos invaden la mucosa intestinal formando lesiones en "cuello de botella". Los organismos enquistan para la mitosis y se pasan a través de las heces.
SÍNTOMAS
Episodios recurrentes de la disentería con sangre y moco en las heces. Hay trastornos gastrointestinales intervinientes y estreñimiento. Los quistes se encuentran en las heces. El organismo puede invadir el hígado, pulmón y cerebro donde se produce abscesos que resultan en disfunción hepática, neumonitis y la encefalitis.
PATOLOGÍA
Úlceras intestinales son debido a la degradación enzimática del tejido.
DIAGNÓSTICO
Examen de parasitos en heces; Deteccion de antigeno en heces. Coprocultivo en medios especiales. En el laboratorio, la infección se confirma al encontrar quistes en las heces. Infección por E. histolytica se distingue de la disentería bacilar por la falta de fiebre alta y ausencia de leucocitosis PMN.
Debe distinguirse de otros protozoos intestinales no patógenas (por ejemplo, Entamoeba coli, Entamoeba hartmanni, fragilis Dientamoeba, Endolimax nana, Iodamoeba buetschlii, etc.).
TRATAMIENTO
Iodoquinol se usa para tratar infecciones asintomáticas y metronidazol se utiliza para amebiasis sintomática y crónica, incluyendo la enfermedad extra-intestinal.
Entamoeba histolytica
Philum: Amoebozoa
Clase: Archamoebae
Orden: Entamoebida
Género y Especie: Entamoeba histolytica
EPIDEMIOLOGÍA
0.5 a 50% de la población mundial alberga parásitos E. histolytica con las tasas más altas de infección en los países subdesarrollados. La infección se asocia con la falta de higiene. Los seres humanos son el principal huésped.
MORFOLOGÍA
Trofozoíto: Forma patogena. Tiene un aspecto ameboide y es por lo general 20 a 50 micrómetros de diámetro. El organismo tiene un único núcleo con un pequeño cariosoma central. El endoplasma granular fino puede contener eritrocitos ingeridos. La cromatina nuclear se distribuye uniformemente por la periferia del núcleo.
Quiste: Forma infectante. Contiene de 1 a 4 núcleos. Son de forma redondeada, refringente con una membrana claramente demarcada. En el citoplasma se pueden ver cuerpos cromatidales.
CICLO DE VIDA
La infección se produce por la ingestión de quistes en los alimentos o las manos con contaminación fecal. El quiste es resistente al medio gástrico y pasa a la intestino delgado, donde eclosiona. El metaquiste se divide en cuatro y luego ocho amebas que se mueven al intestino grueso. La mayoría de los organismos se hacen pasar fuera del cuerpo con las heces, pero, si las condiciones son propicias los trofozoítos invaden la mucosa intestinal formando lesiones en "cuello de botella". Los organismos enquistan para la mitosis y se pasan a través de las heces.
SÍNTOMAS
Episodios recurrentes de la disentería con sangre y moco en las heces. Hay trastornos gastrointestinales intervinientes y estreñimiento. Los quistes se encuentran en las heces. El organismo puede invadir el hígado, pulmón y cerebro donde se produce abscesos que resultan en disfunción hepática, neumonitis y la encefalitis.
PATOLOGÍA
Úlceras intestinales son debido a la degradación enzimática del tejido.
DIAGNÓSTICO
Examen de parasitos en heces; Deteccion de antigeno en heces. Coprocultivo en medios especiales. En el laboratorio, la infección se confirma al encontrar quistes en las heces. Infección por E. histolytica se distingue de la disentería bacilar por la falta de fiebre alta y ausencia de leucocitosis PMN.
Debe distinguirse de otros protozoos intestinales no patógenas (por ejemplo, Entamoeba coli, Entamoeba hartmanni, fragilis Dientamoeba, Endolimax nana, Iodamoeba buetschlii, etc.).
TRATAMIENTO
Iodoquinol se usa para tratar infecciones asintomáticas y metronidazol se utiliza para amebiasis sintomática y crónica, incluyendo la enfermedad extra-intestinal.
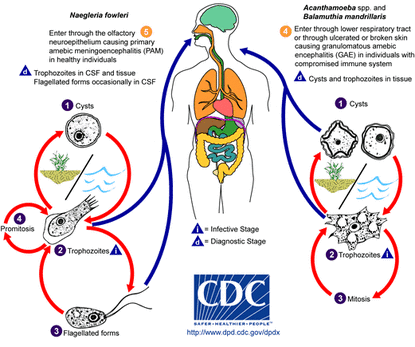
AMEBAS DE VIDA LIBRE
Tres géneros de amebas de vida libre Naegleria, Acanthamoeba, y Balamuthia mandrillaris, son conocidos por infectar a los humanos. Naegleria fowleri causa una encefalitis aguda y casi invariablemente fatal, pero rara. Varias especies de Acanthamoeba y B mandrillaris pueden causar infecciones pulmonares y de la piel, así como una encefalitis insidiosa, en pacientes inmunocomprometidos. Además, Acanthamoeba puede causar una queratitis ulcerativa. Estas amebas viven libremente en el suelo y en las aguas dulces y costeras.
Naegleria fowleri
El organismo se encuentra en todo el mundo en el suelo y el agua dulce caliente. Quistes infecciosos podrán ser transportados en polvo.
MANIFESTACIÓN CLÍNICA
Naegleria fowleri causa meningoencefalitis amebiana primaria, una enfermedad rara, rápidamente fatal con la aparición repentina de dolor de cabeza, fiebre, cuello rígido, letargo y coma en personas por lo demás sanas.
ESTRUCTURA
Los trofozoítos son de 15 a 25µm de diámetro. Los quistes son de una sola pared, esférica y de 8 a 12µm de diámetro. Los trofozoítos pueden también transformarse en una forma flagelada.
PATOGENESIS
Amebas salpicados o inhalados en el epitelio olfativo migran hasta el nervio olfatorio al cerebro y se propagan a través del espacio subaracnoideo.
DIAGNÓSTICO
El diagnóstico se basa en la identificación de trofozoítos por examen microscópico de muestras de líquido cefalorraquídeo frescas o secciones histológicas de tejido del SNC, y en el cultivo, si es necesario.
Acanthamoeba spp
MANIFESTACIÓN CLÍNICA
Especies de Acanthamoeba y Balamuthia mandrillaris suelen actuar como patógenos oportunistas en pacientes inmunocomprometidos o debilitados en los que causan neumonitis o ulceraciones dérmicas. A partir de estas lesiones las amebas pueden propagarse al cerebro para causar una encefalitis insidiosa, lentamente progresiva, y por lo general fatal llamada encefalitis amebiana granulomatosa. En individuos sanos, Acanthamoeba spp puede causar una queratitis ulcerativa, que se asocia a menudo con el uso de lentes de contacto inadecuadamente esterilizados.
ESTRUCTURA
Los trofozoítos son de 15 a 45µm de diámetro con característica pseudópodos en forma de espina. Los quistes son de doble pared, por lo general poligonal y esférica, y 8 a 25 µm de diámetro.
MULTIPLICACIÓN Y CICLO DE VIDA
Los trofozoítos son habitantes de vida libre de tierra y de agua dulce y salada. Se reproducen por fisión binaria.
PATOGÉNESIS
La encefalitis es causada por la diseminación hematógena de lesiones superficiales o pulmonares en el cerebro. La queratitis resulta de la contaminación de las abrasiones corneales superficiales.
DIAGNÓSTICO
El diagnóstico es por lo general mediante el examen microscópico de muestras de biopsia de las lesiones; ambos trofozoítos y quistes pueden ser vistos. Amebas también puede ser cultivado.
TRATAMIENTO
Anfotericina B: intrarraquidea+IV
Tres géneros de amebas de vida libre Naegleria, Acanthamoeba, y Balamuthia mandrillaris, son conocidos por infectar a los humanos. Naegleria fowleri causa una encefalitis aguda y casi invariablemente fatal, pero rara. Varias especies de Acanthamoeba y B mandrillaris pueden causar infecciones pulmonares y de la piel, así como una encefalitis insidiosa, en pacientes inmunocomprometidos. Además, Acanthamoeba puede causar una queratitis ulcerativa. Estas amebas viven libremente en el suelo y en las aguas dulces y costeras.
Naegleria fowleri
El organismo se encuentra en todo el mundo en el suelo y el agua dulce caliente. Quistes infecciosos podrán ser transportados en polvo.
MANIFESTACIÓN CLÍNICA
Naegleria fowleri causa meningoencefalitis amebiana primaria, una enfermedad rara, rápidamente fatal con la aparición repentina de dolor de cabeza, fiebre, cuello rígido, letargo y coma en personas por lo demás sanas.
ESTRUCTURA
Los trofozoítos son de 15 a 25µm de diámetro. Los quistes son de una sola pared, esférica y de 8 a 12µm de diámetro. Los trofozoítos pueden también transformarse en una forma flagelada.
PATOGENESIS
Amebas salpicados o inhalados en el epitelio olfativo migran hasta el nervio olfatorio al cerebro y se propagan a través del espacio subaracnoideo.
DIAGNÓSTICO
El diagnóstico se basa en la identificación de trofozoítos por examen microscópico de muestras de líquido cefalorraquídeo frescas o secciones histológicas de tejido del SNC, y en el cultivo, si es necesario.
Acanthamoeba spp
MANIFESTACIÓN CLÍNICA
Especies de Acanthamoeba y Balamuthia mandrillaris suelen actuar como patógenos oportunistas en pacientes inmunocomprometidos o debilitados en los que causan neumonitis o ulceraciones dérmicas. A partir de estas lesiones las amebas pueden propagarse al cerebro para causar una encefalitis insidiosa, lentamente progresiva, y por lo general fatal llamada encefalitis amebiana granulomatosa. En individuos sanos, Acanthamoeba spp puede causar una queratitis ulcerativa, que se asocia a menudo con el uso de lentes de contacto inadecuadamente esterilizados.
ESTRUCTURA
Los trofozoítos son de 15 a 45µm de diámetro con característica pseudópodos en forma de espina. Los quistes son de doble pared, por lo general poligonal y esférica, y 8 a 25 µm de diámetro.
MULTIPLICACIÓN Y CICLO DE VIDA
Los trofozoítos son habitantes de vida libre de tierra y de agua dulce y salada. Se reproducen por fisión binaria.
PATOGÉNESIS
La encefalitis es causada por la diseminación hematógena de lesiones superficiales o pulmonares en el cerebro. La queratitis resulta de la contaminación de las abrasiones corneales superficiales.
DIAGNÓSTICO
El diagnóstico es por lo general mediante el examen microscópico de muestras de biopsia de las lesiones; ambos trofozoítos y quistes pueden ser vistos. Amebas también puede ser cultivado.
TRATAMIENTO
Anfotericina B: intrarraquidea+IV
CILIADO
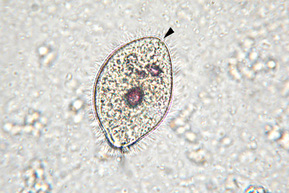 Wet mount.
En este trofozoíto, los cilios son vistos fácilmente.
Wet mount.
En este trofozoíto, los cilios son vistos fácilmente.
BALANTIDIASIS
Balantidium coli
Philum: Ciliophora
Clase: Litostomatea
Orden: Vestibuliferida
Género y Especie: Balantidium Coli
Este es un parásito ciliado principalmente de vacas, cerdos y caballos. El organismo es un grande (100 x 60 micrómetros) ciliado con una macro y un micro-núcleo. La infección ocurre principalmente en los trabajadores agrícolas y otros habitantes de zonas rurales por la ingestión de quistes en la materia fecal de los animales de granja.
CLÍNICA
Puede ser asintomática o asociada a dolor abdominal, diarreas crónicas intermitentes y pérdida de peso. En algunos casos puede dar lugar a un cuadro de disentería fulminante.
Síntomas y patogénesis de balantidiasis son similares a los observados en entamebiasis, incluyendo erosión epitelial intestinal. Sin embargo, hígado, pulmón y cerebro abscesos no se ven. Afecta al intestino grueso y tramo final del ileon. Capacidad invasiva con formacion de necrosis y ulceras (semejante a ulceras amebianas).
DIAGNÓSTICO
Identificacion del parasito en heces.
TRATAMIENTO
Tinidazol y Ornidazol. Alternativas: metronidazol
Balantidium coli
Philum: Ciliophora
Clase: Litostomatea
Orden: Vestibuliferida
Género y Especie: Balantidium Coli
Este es un parásito ciliado principalmente de vacas, cerdos y caballos. El organismo es un grande (100 x 60 micrómetros) ciliado con una macro y un micro-núcleo. La infección ocurre principalmente en los trabajadores agrícolas y otros habitantes de zonas rurales por la ingestión de quistes en la materia fecal de los animales de granja.
CLÍNICA
Puede ser asintomática o asociada a dolor abdominal, diarreas crónicas intermitentes y pérdida de peso. En algunos casos puede dar lugar a un cuadro de disentería fulminante.
Síntomas y patogénesis de balantidiasis son similares a los observados en entamebiasis, incluyendo erosión epitelial intestinal. Sin embargo, hígado, pulmón y cerebro abscesos no se ven. Afecta al intestino grueso y tramo final del ileon. Capacidad invasiva con formacion de necrosis y ulceras (semejante a ulceras amebianas).
DIAGNÓSTICO
Identificacion del parasito en heces.
TRATAMIENTO
Tinidazol y Ornidazol. Alternativas: metronidazol
FLAGELADOS
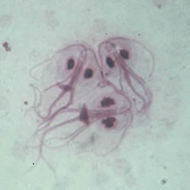 Trofozoito
Trofozoito
GIARDIASIS
Giardia lamblia
Philum: Metamonada
Clase: Eopharyngia
Orden: Diplomonadida
Género y Especie: Giardia lamblia
EPIDEMIOLOGÍA
Tiene distribución en todo el mundo. Es la enfermedad intestinal protozoario más frecuente y la causa identificada más común de las enfermedades transmitidas por el agua asociada con la ruptura de los sistemas de purificación de agua.
MORFOLOGÍA
Trofozoito: G. lamblia es un organismo de 12 a 15 micrómetros, en forma de pera con 8 flagelos y 2 axostilos dispuestos en una simetría bilateral. Hay dos discos de succión grandes localizados anteriormente. El citoplasma contiene dos núcleos y dos cuerpos parabasales.
Quiste: Son células elipsoidales de 9 a 12 micrómetro. El citoplasma contiene cuatro núcleos y muchas de las estructuras observadas en el trofozoítos.
CICLO DE VIDA
La infección se produce por la ingestión de quistes, por lo general en el agua contaminada. El quiste se eclosiona en el duodeno y trofozoítos colonizan el intestino delgado superior, donde pueden nadar libremente o adjuntar al epitelio submucosa a través del disco de succión ventral. Los trofozoítos libres se enquistan nuevamente y la mitosis tiene lugar durante el enquistamiento. Los quistes se pasan en las heces. El hombre es el huésped primario aunque castores, los cerdos y los monos también están infectadas y sirven como reservorios.
SÍNTOMAS
Los primeros síntomas incluyen flatulencia, distensión abdominal, náuseas y diarrea maloliente voluminosa, explosivo, a menudo acuosa. La materia fecal contiene lípidos excesivos pero muy rara vez sangre o tejido necrótico. La fase más crónica se asocia con la malabsorción de vitamina B12, deficiencia disacaridasa y la intolerancia a la lactosa.
PATOLOGÍA
Cubrir el epitelio intestinal por el trophozoite y aplanamiento del superficie de la mucosa resulta en la mala absorción de nutrientes.
DIAGNÓSTICO
la disentería a cause de G. lamblia es distinta de otras disenterías debido a la falta de moco y sangre en las heces, la falta de aumento de los leucocitos PMN en las heces y la falta de fiebre alta. Los quistes en las heces y trophozoites en el duodeno se pueden identificar microscópicamente para confirmar el diagnostico.
TRATAMIENTO
El metronidazol es el fármaco de elección.
Giardia lamblia
Philum: Metamonada
Clase: Eopharyngia
Orden: Diplomonadida
Género y Especie: Giardia lamblia
EPIDEMIOLOGÍA
Tiene distribución en todo el mundo. Es la enfermedad intestinal protozoario más frecuente y la causa identificada más común de las enfermedades transmitidas por el agua asociada con la ruptura de los sistemas de purificación de agua.
MORFOLOGÍA
Trofozoito: G. lamblia es un organismo de 12 a 15 micrómetros, en forma de pera con 8 flagelos y 2 axostilos dispuestos en una simetría bilateral. Hay dos discos de succión grandes localizados anteriormente. El citoplasma contiene dos núcleos y dos cuerpos parabasales.
Quiste: Son células elipsoidales de 9 a 12 micrómetro. El citoplasma contiene cuatro núcleos y muchas de las estructuras observadas en el trofozoítos.
CICLO DE VIDA
La infección se produce por la ingestión de quistes, por lo general en el agua contaminada. El quiste se eclosiona en el duodeno y trofozoítos colonizan el intestino delgado superior, donde pueden nadar libremente o adjuntar al epitelio submucosa a través del disco de succión ventral. Los trofozoítos libres se enquistan nuevamente y la mitosis tiene lugar durante el enquistamiento. Los quistes se pasan en las heces. El hombre es el huésped primario aunque castores, los cerdos y los monos también están infectadas y sirven como reservorios.
SÍNTOMAS
Los primeros síntomas incluyen flatulencia, distensión abdominal, náuseas y diarrea maloliente voluminosa, explosivo, a menudo acuosa. La materia fecal contiene lípidos excesivos pero muy rara vez sangre o tejido necrótico. La fase más crónica se asocia con la malabsorción de vitamina B12, deficiencia disacaridasa y la intolerancia a la lactosa.
PATOLOGÍA
Cubrir el epitelio intestinal por el trophozoite y aplanamiento del superficie de la mucosa resulta en la mala absorción de nutrientes.
DIAGNÓSTICO
la disentería a cause de G. lamblia es distinta de otras disenterías debido a la falta de moco y sangre en las heces, la falta de aumento de los leucocitos PMN en las heces y la falta de fiebre alta. Los quistes en las heces y trophozoites en el duodeno se pueden identificar microscópicamente para confirmar el diagnostico.
TRATAMIENTO
El metronidazol es el fármaco de elección.
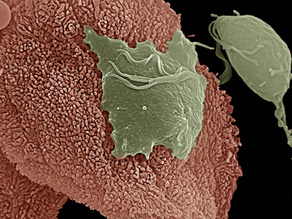 Una micrografía electrónica muestra el parásito T. vaginalis adhiriéndose a las células epiteliales vaginales recogidas de muestras vaginales.
Una micrografía electrónica muestra el parásito T. vaginalis adhiriéndose a las células epiteliales vaginales recogidas de muestras vaginales.
TRICOMONIASIS
Trichomonas vaginalis
MORFOLOGÍA
La forma trophozoite es de 7×10 micrómetros de diámetro y es en forma de pera con un solo núcleo, cuatro flagelos anterior y un flagelo lateral unida por una membrana ondulante. El organismo no enquista.
CICLO DE VIDA
T. vaginalis coloniza la vagina de la mujer y la uretra (a veces de próstata) de los hombres. La infección se produce principalmente a través del contacto sexual, aunque las infecciones no venéreas son posibles. El organismo no enquista y se divide por fisión binaria que se ve favorecida por una baja acidez. No hay reservorio no humano.
SÍNTOMAS
La infección por T. vaginalis es rara vez sintomática en los hombres, aunque puede causar uretritis leve o en ocasiones la prostatitis. En las mujeres, a menudo es asintomática, pero las infecciones graves en un entorno de alto pH puede causar de leve a grave vaginitis con descarga copiosa amarillento de olor fétido, a veces espumosa.
DIAGNÓSTICO
La sospecha clínica se puede confirmar mediante la búsqueda del organismo en los frotis teñidos con Giemsa de la secreción vaginal. Trofozoítos deben distinguirse de la Trichomona hominis flagelado no patógena.
TRATAMIENTO Y CONTROL
El metronidazol (aunque teratogénico) es eficaz tanto en hombres como en mujeres. La higiene personal y el uso de los condones son útiles.
Trichomonas vaginalis
MORFOLOGÍA
La forma trophozoite es de 7×10 micrómetros de diámetro y es en forma de pera con un solo núcleo, cuatro flagelos anterior y un flagelo lateral unida por una membrana ondulante. El organismo no enquista.
CICLO DE VIDA
T. vaginalis coloniza la vagina de la mujer y la uretra (a veces de próstata) de los hombres. La infección se produce principalmente a través del contacto sexual, aunque las infecciones no venéreas son posibles. El organismo no enquista y se divide por fisión binaria que se ve favorecida por una baja acidez. No hay reservorio no humano.
SÍNTOMAS
La infección por T. vaginalis es rara vez sintomática en los hombres, aunque puede causar uretritis leve o en ocasiones la prostatitis. En las mujeres, a menudo es asintomática, pero las infecciones graves en un entorno de alto pH puede causar de leve a grave vaginitis con descarga copiosa amarillento de olor fétido, a veces espumosa.
DIAGNÓSTICO
La sospecha clínica se puede confirmar mediante la búsqueda del organismo en los frotis teñidos con Giemsa de la secreción vaginal. Trofozoítos deben distinguirse de la Trichomona hominis flagelado no patógena.
TRATAMIENTO Y CONTROL
El metronidazol (aunque teratogénico) es eficaz tanto en hombres como en mujeres. La higiene personal y el uso de los condones son útiles.
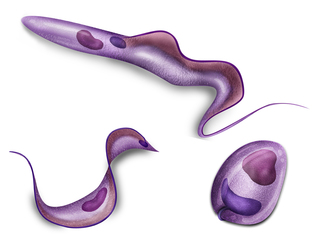
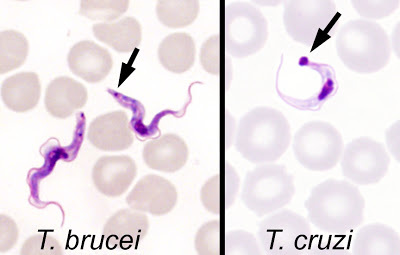
TRIPANOSOMIASIS
Philum: Euglenozoa
Clase: Zoomastigophora
Orden: Trypanosomatida
Género: Trypanosoma
Enfermedad de Chagas
Causada por el protozoo hemoflagelado, Trypanosoma cruzi.
EPIDEMIOLOGÍA
Tripanosomiasis americana, también conocida como enfermedad de Chagas, se dispersa irregularmente en América Central y del Sur, que se extiende a partir de partes de México a Argentina.
MORFOLOGÍA
El organismo se produce en tres formas diferentes, dependiendo de su entorno. Tripomastigote: forma fusiforme, 15 a 20µm de largo, con el extremo posterior en punta, con un kinetoplasto posterior al núcleo de donde emerge una membrana ondulante que recorre el cuerpo y termina en un flagelo libre. Es la forma en que se encuentra en la sangre de los mamíferos y en la parte posterior del intestino de los triatómidos. Es la forma infectante. Amastigote: se encuentra intracelularmente o en pseudoquistes en las vísceras de mamífero (particularmente en el miocardio y el cerebro), es redonda u ovalada, mide 2-4µm y carece de un flagelo prominente. Epimastigote: es la forma de multiplicación en el intestino del triatómido y la predominante en los medios de cultivo.
CICLO DE VIDA
El microorganismo se transmite al huésped mamífero por muchas especies vinchuca (riduvid), lo más prominente por Triatoma infestans, y T. sordida. Transmisión tiene lugar durante la alimentación del insecto que normalmente muerde en la zona facial y tiene el hábito de defecar durante la alimentación. Los tripomastigotes metacíclicas, contenidas en el material fecal, accede a los tejidos de los mamíferos a través de la herida que a menudo se frota por el individuo que fuere mordido. Posteriormente, entran en diversas células, incluyendo macrófagos, donde se diferencian en amastigotes y se multiplican por fisión binaria. Los amastigotes se diferencian en mas tripomastigotes y las células se rompen para liberarlos al torrente sanguíneo. Células huésped adicionales, de una gran variedad, pueden infectarse y los tripomastigotes formar una vez más amastigotes dentro de estas células. Insectos vectores no infectados adquieren el organismo cuando se alimentan de animales infectados o personas que contienen tripomastigotes circulantes en la sangre. En el interior del tubo digestivo del vector, los tripomastigotes se diferencian para formar epimastigotes y estos se dividen en el intestino posterior del insecto donde se transforman en tripomastigotes metacíclicos infecciosos. La transmisión también puede producirse de hombre a hombre por la transfusión de sangre y por vía transplacentaria.
Más de un centenar de especies de mamíferos de los animales salvajes y domésticos, incluyendo el ganado, cerdos, gatos, perros, ratas, armadillos, mapaches y zarigüeyas son naturalmente infectadas por T. cruzi y serven como reservorio.
LOS SÍNTOMAS
La enfermedad de Chagas se puede dividir en tres etapas: la lesión primaria, la etapa aguda y la fase crónica. La lesión primaria, chagoma, apareciendo en el sitio de la infección, consiste en una ligeramente elevada, placa eritematosa no purulenta plana rodeada por una zona variable de edema duro. Se encuentra generalmente en la cara, los párpados, las mejillas, los labios o la conjuntiva, pero puede ocurrir en el abdomen o en las extremidades. La infección en el párpado, dando como resultado una conjuntivitis unilateral y edema orbital (signo de Romana), es el hallazgo más común.
Etapa aguda: Aparece 7-14 días después de la infección. Se caracteriza por inquietud, insomnio, malestar general, aumento el cansancio, escalofríos, fiebre y dolores óseos y musculares. Otras manifestaciones son adenitis cervical, axilar y ilíaca, hepatomegalia, exantema eritematoso y miocarditis aguda. Hay una reacción edematosa general asociada con la linfadenopatía. Miocarditis difusa, a veces acompañada de la pericarditis y endocarditis graves, es muy frecuente durante la etapa inicial de la enfermedad. En los niños, la enfermedad puede causar meningoencefalitis y coma. La muerte ocurre en el 5-10 por ciento de los recién nacidos.
Fase crónica: La etapa aguda por lo general no se reconoce y, a menudo se resuelve con poco o ningún daño inmediato y el huésped infectado sigue siendo un portador asintomático. Los pacientes crónicas alternan entre períodos de remisión asintomática y recaídas que se caracterizan por síntomas que se observan en la fase aguda. Arritmia cardiaca es común. Los resultados de la enfermedad crónica en una función anormal de los órganos huecos, en particular el corazón, el esófago y el colon. Los cambios cardíacos incluyen insuficiencia miocárdica, cardiomegalia, alteraciones de la conducción aurículo-ventricular y el síndrome de Adams-Stoke. Las formas crónicas digestivas incluyen megaesófago y megacolon.
DIAGNÓSTICO
El diagnóstico clínico es generalmente fácil entre los niños de zonas endémicas. dilatación Cardiaca, megacolon y megaesófago en individuos de zonas endémicas indican infección actual o anterior. El diagnóstico definitivo requiere la demostración de tripanosomas por microscopía o análisis bioquímicos, los anticuerpos son detectables a menudo por fijación del complemento o inmunofluorescencia y proporcionan diagnóstico presuntivo.
TRATAMIENTO Y CONTROL
Benznidazol y Nifurtimox se han utilizado con resultados prometedores en la fase aguda de la enfermedad, sin embargo sus efectos secundarios limitan su uso prolongado en los casos crónicos.
Las medidas de control se limitan a los que reducir el contacto entre los vectores y el hombre.
La Tripanosomiasis Africana (Enfermedad del Sueño)
ETIOLOGÍA
Hay dos formas clínicas de la tripanosomiasis africana: 1) una enfermedad de desarrollo lento causada por Trypanosoma brucei gambiense y 2) una enfermedad que progresa rápidamente causada por T. brucei rhodesiense.
EPIDEMIOLOGÍA
T. b. gambiense es predominante en las regiones occidental y central de África, mientras que T. b. rhodesiense se limita al tercio oriental del continente.
MORFOLOGÍA
T. b. gambiense y T. b. rhodesiense son similares en apariencia: El organismo mide 10-30 x 1-3 micrómetros. Tiene un único núcleo central y un solo flagelo que se origina en el cinetoplasto y se une al cuerpo por una membrana ondulante.
CICLO DE VIDA
LOS SÍNTOMAS
Las características clínicas de la enfermedad de Gambia y Rodesia son los mismos, sin embargo, varían en gravedad y duración. Enfermedad Rhodesian progresa más rápidamente y los síntomas son a menudo más pronunciados. Clásicamente, la progresión de la tripanosomiasis africana se puede dividir en tres etapas: la reacción de mordida (chancro), parasitemia (sangre y los tejidos linfoides), y la etapa del SNC. Las características clínicas de la enfermedad de Rhodesia son similares pero más breves y más agudas.
DIAGNÓSTICO
La detección de parásitos en el torrente sanguíneo, aspirado de secreciones ganglionares y nodos linfáticos agrandado proporciona un diagnóstico definitivo en etapas tempranas (aguda).
TRATAMIENTO Y CONTROL
Suramina, Melasoprol, y Pentamidina
El medio más eficaz de prevención es evitar el contacto con las moscas tsetsé. La erradicación del vector es poco práctica debido a la gran área involucrada.
Philum: Euglenozoa
Clase: Zoomastigophora
Orden: Trypanosomatida
Género: Trypanosoma
Enfermedad de Chagas
Causada por el protozoo hemoflagelado, Trypanosoma cruzi.
EPIDEMIOLOGÍA
Tripanosomiasis americana, también conocida como enfermedad de Chagas, se dispersa irregularmente en América Central y del Sur, que se extiende a partir de partes de México a Argentina.
MORFOLOGÍA
El organismo se produce en tres formas diferentes, dependiendo de su entorno. Tripomastigote: forma fusiforme, 15 a 20µm de largo, con el extremo posterior en punta, con un kinetoplasto posterior al núcleo de donde emerge una membrana ondulante que recorre el cuerpo y termina en un flagelo libre. Es la forma en que se encuentra en la sangre de los mamíferos y en la parte posterior del intestino de los triatómidos. Es la forma infectante. Amastigote: se encuentra intracelularmente o en pseudoquistes en las vísceras de mamífero (particularmente en el miocardio y el cerebro), es redonda u ovalada, mide 2-4µm y carece de un flagelo prominente. Epimastigote: es la forma de multiplicación en el intestino del triatómido y la predominante en los medios de cultivo.
CICLO DE VIDA
El microorganismo se transmite al huésped mamífero por muchas especies vinchuca (riduvid), lo más prominente por Triatoma infestans, y T. sordida. Transmisión tiene lugar durante la alimentación del insecto que normalmente muerde en la zona facial y tiene el hábito de defecar durante la alimentación. Los tripomastigotes metacíclicas, contenidas en el material fecal, accede a los tejidos de los mamíferos a través de la herida que a menudo se frota por el individuo que fuere mordido. Posteriormente, entran en diversas células, incluyendo macrófagos, donde se diferencian en amastigotes y se multiplican por fisión binaria. Los amastigotes se diferencian en mas tripomastigotes y las células se rompen para liberarlos al torrente sanguíneo. Células huésped adicionales, de una gran variedad, pueden infectarse y los tripomastigotes formar una vez más amastigotes dentro de estas células. Insectos vectores no infectados adquieren el organismo cuando se alimentan de animales infectados o personas que contienen tripomastigotes circulantes en la sangre. En el interior del tubo digestivo del vector, los tripomastigotes se diferencian para formar epimastigotes y estos se dividen en el intestino posterior del insecto donde se transforman en tripomastigotes metacíclicos infecciosos. La transmisión también puede producirse de hombre a hombre por la transfusión de sangre y por vía transplacentaria.
Más de un centenar de especies de mamíferos de los animales salvajes y domésticos, incluyendo el ganado, cerdos, gatos, perros, ratas, armadillos, mapaches y zarigüeyas son naturalmente infectadas por T. cruzi y serven como reservorio.
LOS SÍNTOMAS
La enfermedad de Chagas se puede dividir en tres etapas: la lesión primaria, la etapa aguda y la fase crónica. La lesión primaria, chagoma, apareciendo en el sitio de la infección, consiste en una ligeramente elevada, placa eritematosa no purulenta plana rodeada por una zona variable de edema duro. Se encuentra generalmente en la cara, los párpados, las mejillas, los labios o la conjuntiva, pero puede ocurrir en el abdomen o en las extremidades. La infección en el párpado, dando como resultado una conjuntivitis unilateral y edema orbital (signo de Romana), es el hallazgo más común.
Etapa aguda: Aparece 7-14 días después de la infección. Se caracteriza por inquietud, insomnio, malestar general, aumento el cansancio, escalofríos, fiebre y dolores óseos y musculares. Otras manifestaciones son adenitis cervical, axilar y ilíaca, hepatomegalia, exantema eritematoso y miocarditis aguda. Hay una reacción edematosa general asociada con la linfadenopatía. Miocarditis difusa, a veces acompañada de la pericarditis y endocarditis graves, es muy frecuente durante la etapa inicial de la enfermedad. En los niños, la enfermedad puede causar meningoencefalitis y coma. La muerte ocurre en el 5-10 por ciento de los recién nacidos.
Fase crónica: La etapa aguda por lo general no se reconoce y, a menudo se resuelve con poco o ningún daño inmediato y el huésped infectado sigue siendo un portador asintomático. Los pacientes crónicas alternan entre períodos de remisión asintomática y recaídas que se caracterizan por síntomas que se observan en la fase aguda. Arritmia cardiaca es común. Los resultados de la enfermedad crónica en una función anormal de los órganos huecos, en particular el corazón, el esófago y el colon. Los cambios cardíacos incluyen insuficiencia miocárdica, cardiomegalia, alteraciones de la conducción aurículo-ventricular y el síndrome de Adams-Stoke. Las formas crónicas digestivas incluyen megaesófago y megacolon.
DIAGNÓSTICO
El diagnóstico clínico es generalmente fácil entre los niños de zonas endémicas. dilatación Cardiaca, megacolon y megaesófago en individuos de zonas endémicas indican infección actual o anterior. El diagnóstico definitivo requiere la demostración de tripanosomas por microscopía o análisis bioquímicos, los anticuerpos son detectables a menudo por fijación del complemento o inmunofluorescencia y proporcionan diagnóstico presuntivo.
TRATAMIENTO Y CONTROL
Benznidazol y Nifurtimox se han utilizado con resultados prometedores en la fase aguda de la enfermedad, sin embargo sus efectos secundarios limitan su uso prolongado en los casos crónicos.
Las medidas de control se limitan a los que reducir el contacto entre los vectores y el hombre.
La Tripanosomiasis Africana (Enfermedad del Sueño)
ETIOLOGÍA
Hay dos formas clínicas de la tripanosomiasis africana: 1) una enfermedad de desarrollo lento causada por Trypanosoma brucei gambiense y 2) una enfermedad que progresa rápidamente causada por T. brucei rhodesiense.
EPIDEMIOLOGÍA
T. b. gambiense es predominante en las regiones occidental y central de África, mientras que T. b. rhodesiense se limita al tercio oriental del continente.
MORFOLOGÍA
T. b. gambiense y T. b. rhodesiense son similares en apariencia: El organismo mide 10-30 x 1-3 micrómetros. Tiene un único núcleo central y un solo flagelo que se origina en el cinetoplasto y se une al cuerpo por una membrana ondulante.
CICLO DE VIDA
LOS SÍNTOMAS
Las características clínicas de la enfermedad de Gambia y Rodesia son los mismos, sin embargo, varían en gravedad y duración. Enfermedad Rhodesian progresa más rápidamente y los síntomas son a menudo más pronunciados. Clásicamente, la progresión de la tripanosomiasis africana se puede dividir en tres etapas: la reacción de mordida (chancro), parasitemia (sangre y los tejidos linfoides), y la etapa del SNC. Las características clínicas de la enfermedad de Rhodesia son similares pero más breves y más agudas.
DIAGNÓSTICO
La detección de parásitos en el torrente sanguíneo, aspirado de secreciones ganglionares y nodos linfáticos agrandado proporciona un diagnóstico definitivo en etapas tempranas (aguda).
TRATAMIENTO Y CONTROL
Suramina, Melasoprol, y Pentamidina
El medio más eficaz de prevención es evitar el contacto con las moscas tsetsé. La erradicación del vector es poco práctica debido a la gran área involucrada.
LEISHMANIASIS
Philum: Sarcomastigophora
Clase: Zoomastigophora
Orden: Kinetplastida
Género: Leishmania
ETIOLOGÍA
Varias especies de Leishmania son patógenas para el hombre: L. donovani causa la leishmaniasis visceral (kala-azar, enfermedad negro); L. tropica causa leishmaniasis cutánea; y L. braziliensis y L. mexicana son agentes etiológicos de leishmaniasis mucocutánea (espundia, Uta, úlcera del chiclero).
EPIDEMIOLOGÍA
La leishmaniasis es prevalente mundialmente: va desde el sudeste de Asia, India y Pakistán, Mediterráneo, el norte y el centro de África, y el sur y centro de América.
MORFOLOGÍA
El amastigote se encuentra intracelularmente, es oval y mide 2.5µm por 1-3µm, mientras que el promastigote mide 14 a 20µm por 1.5-4 µm, es extracelular y la forma en que se encuentra en el intestino del vector y en los cultivos “in vitro”
CICLO DE VIDA
El microorganismo se transmite por la picadura de varias especies de moscas de arena (Phlebotomus) que se alimentan del sangre del huésped y que llevan la promastigote en su intestino anterior y faringe. Los parásitos ganan obtienen acceso a los fagocitos mononucleares en donde se transforman en amastigotes y se dividen hasta que se rompe la célula infectada. Los organismos liberados infectan a otras células. El flebótomo adquiere los organismos durante alimentarse de sangre; los amastigotes se transforman en promastigotes flagelados y se multiplican en el intestino hasta que el intestino anterior y la faringe se embalan. Los perros y los roedores son los reservorios comunes.
SÍNTOMAS
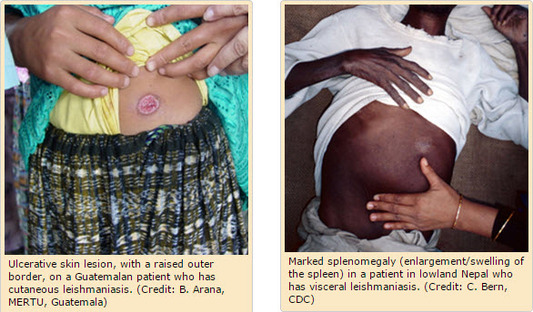
Leishmaniasis visceral (kala-azar “enfermedad negro”): los organismos de L. donovani se eliminan rápidamente del sitio de la infección, por lo tanto, rara vez hay una lesión local. Se localizan y se multiplican en las células fagocíticas mononucleares del bazo, hígado, ganglios linfáticos, médula ósea, mucosa intestinal y otros órganos. Progresivamente ocurre la hepatoesplenomegalia. Con la progresión de la enfermedad, la piel desarrolla áreas granulomatosas hiperpigmentadas.
Leishmaniasis cutánea: el organismo (L. tropica) multiplica localmente, produciendo de una pápula, 1-2 semanas (o tan largo como 1-2 meses) después de la picadura. La pápula crece gradualmente para formar una úlcera relativamente indolora. El centro de la úlcera incrusta mientras pápulas satélites desarrollan en la periferia. Los úlcera se cura en 2-10 meses, aunque no tratadas, pero deja una cicatriz que desfigura. La enfermedad puede difundir en el caso de la función inmune deprimida.
Leishmaniasis mucocutánea (espundia, Uta, chiclero): los síntomas iniciales de la leishmaniasis mucocutánea son los mismos que los de la leishmaniasis cutánea, excepto que en esta enfermedad el organismo pueden hacer metástasis y las lesiones se extienden a los tejidos mucoide (oral, faríngea y nasal) y provocar su destrucción y, por tanto, deformidad severa.
DIAGNÓSTICO
Se basa en el aislamiento de los organismos de la aspiración o biopsia de la lesión, mediante un examen o cultivo directo. Una prueba de la piel (hipersensibilidad retardada: test Montenegro) y la detección de anticuerpos anti-Leishmania por inmunofluorescencia son indicativos de exposición.
TRATAMIENTO
Antimonio pentavalente. El isetionato de pentamidina se utiliza como una alternativa.
Philum: Sarcomastigophora
Clase: Zoomastigophora
Orden: Kinetplastida
Género: Leishmania
ETIOLOGÍA
Varias especies de Leishmania son patógenas para el hombre: L. donovani causa la leishmaniasis visceral (kala-azar, enfermedad negro); L. tropica causa leishmaniasis cutánea; y L. braziliensis y L. mexicana son agentes etiológicos de leishmaniasis mucocutánea (espundia, Uta, úlcera del chiclero).
EPIDEMIOLOGÍA
La leishmaniasis es prevalente mundialmente: va desde el sudeste de Asia, India y Pakistán, Mediterráneo, el norte y el centro de África, y el sur y centro de América.
MORFOLOGÍA
El amastigote se encuentra intracelularmente, es oval y mide 2.5µm por 1-3µm, mientras que el promastigote mide 14 a 20µm por 1.5-4 µm, es extracelular y la forma en que se encuentra en el intestino del vector y en los cultivos “in vitro”
CICLO DE VIDA
El microorganismo se transmite por la picadura de varias especies de moscas de arena (Phlebotomus) que se alimentan del sangre del huésped y que llevan la promastigote en su intestino anterior y faringe. Los parásitos ganan obtienen acceso a los fagocitos mononucleares en donde se transforman en amastigotes y se dividen hasta que se rompe la célula infectada. Los organismos liberados infectan a otras células. El flebótomo adquiere los organismos durante alimentarse de sangre; los amastigotes se transforman en promastigotes flagelados y se multiplican en el intestino hasta que el intestino anterior y la faringe se embalan. Los perros y los roedores son los reservorios comunes.
SÍNTOMAS
Leishmaniasis visceral (kala-azar “enfermedad negro”): los organismos de L. donovani se eliminan rápidamente del sitio de la infección, por lo tanto, rara vez hay una lesión local. Se localizan y se multiplican en las células fagocíticas mononucleares del bazo, hígado, ganglios linfáticos, médula ósea, mucosa intestinal y otros órganos. Progresivamente ocurre la hepatoesplenomegalia. Con la progresión de la enfermedad, la piel desarrolla áreas granulomatosas hiperpigmentadas.
Leishmaniasis cutánea: el organismo (L. tropica) multiplica localmente, produciendo de una pápula, 1-2 semanas (o tan largo como 1-2 meses) después de la picadura. La pápula crece gradualmente para formar una úlcera relativamente indolora. El centro de la úlcera incrusta mientras pápulas satélites desarrollan en la periferia. Los úlcera se cura en 2-10 meses, aunque no tratadas, pero deja una cicatriz que desfigura. La enfermedad puede difundir en el caso de la función inmune deprimida.
Leishmaniasis mucocutánea (espundia, Uta, chiclero): los síntomas iniciales de la leishmaniasis mucocutánea son los mismos que los de la leishmaniasis cutánea, excepto que en esta enfermedad el organismo pueden hacer metástasis y las lesiones se extienden a los tejidos mucoide (oral, faríngea y nasal) y provocar su destrucción y, por tanto, deformidad severa.
DIAGNÓSTICO
Se basa en el aislamiento de los organismos de la aspiración o biopsia de la lesión, mediante un examen o cultivo directo. Una prueba de la piel (hipersensibilidad retardada: test Montenegro) y la detección de anticuerpos anti-Leishmania por inmunofluorescencia son indicativos de exposición.
TRATAMIENTO
Antimonio pentavalente. El isetionato de pentamidina se utiliza como una alternativa.
ESPOROZOOS
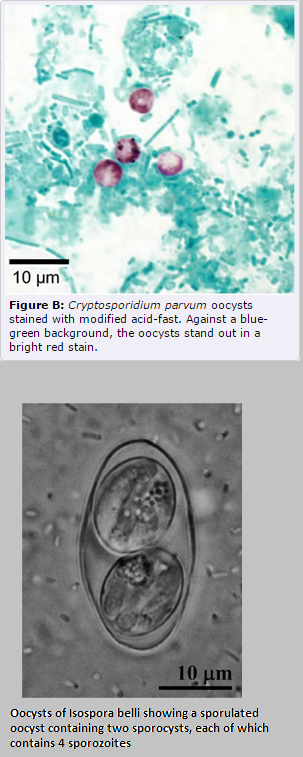
CRIPTOSPORIDIOSIS
Philum: Apicomplexa
Clase: Sporozoasida
Orden: Eucoccidiorida
Género y Especie: Cryptosporidium parvum
C. parvum es un parásito pequeño y redondo de medición 3 a 5 micrómetros que se encuentra en el tracto gastrointestinal de muchos animales y causa epidemias de diarrea en los seres humanos a través de alimentos y agua contaminada.
Los seres humanos se infectan por la ingestión de ooquistes C. parvum que contienen muchos esporozoitos. Los esporozoítos se liberan en el tracto gastrointestinal superior y se unen a las células de la mucosa intestinal, donde se dividen para producir merozoitos. Los merozoitos invaden otras células de la mucosa y se multiplican asexualmente. Algunos de los merozoitos se diferencian en gametocitos masculinos y femeninos y forman un ooquistes en el que se multiplican y se diferencian en esporozoitos. El ooquiste maduro se excreta con la materia fecal e infecta a otros individuos.
CLÍNICA.
Asintomatica. Diarrea aguda autolimitada (inmunocompetentes) o cronica en ocaciones con compromiso vital (inmunodeficientes). Localizacion extraintestinal, en ocasiones, especialmente en pacientes inmunodeficientes, que puede ocasionar colecistitis alitiasica, colangitis, pancreatitis, hepatitis.
DIAGNÓSTICO.
Identificación de los quistes del parasito en las heces. Técnicas de concentración. Tinción de Kinyoun. Detección de antígeno en heces. Visualización de ooquistes en biopsia yeyunal.
TRATAMIENTO.
Autolimitada en inmunocompetentes, no requiere tratamiento. Inmunodeprimidos: correccion de la inmunodeficiencia. El tratamiento especifico no elimina la infeccion, pero reduce la gravedad del cuadro. Nitazoxamida y Paramomicina.
Alternativas: en los casos cronicos rebeldes al tratamiento son importantes las medidas de rehidratacion y tratamiento sintomatico con antiperistalticos y analogos de la somatostatina.
ISOSPORIASIS
Isospora belli
I. belli es protozoo que afecta al intestino delgado. Es cosmopolita y las personas se infectan al ingerir agua o alimentos contaminados con ooquistes maduros.
Tiene una capacidad invasiva. Es una infección poco común de los humanos sana, a pesar de que está siendo visto en número creciente en pacientes con SIDA. La infección se produce por vía oro-fecal. La etapa infecciosa del organismo es un oocisto ovalada que, después de la ingestión, sigue el mismo curso que C. parvum. En individuos normales, infecciones leves se resuelven con reposo y dieta suave y las infecciones más graves pueden ser tratados con medicamentos sulfa. El tratamiento puede tener que ser llevado a cabo durante un período prolongado en pacientes con SIDA.
CLÍNICA.
Asintomatica. Diarrea, flatulencia, colico abdominal, anorexia, febrícula, pérdida de peso. Puede producir eosinofilia periferica. En personas inmunocompetentes suele producir una enfermedad autolimitada. En inmunodeprimidos se cronifica.
DIAGNÓSTICO.
Identificacion del parasito en las heces. Tinciones de Kinyoun.
TRATAMIENTO.
Trimetoprim-Sulfametoxazol (TMS).
Philum: Apicomplexa
Clase: Sporozoasida
Orden: Eucoccidiorida
Género y Especie: Cryptosporidium parvum
C. parvum es un parásito pequeño y redondo de medición 3 a 5 micrómetros que se encuentra en el tracto gastrointestinal de muchos animales y causa epidemias de diarrea en los seres humanos a través de alimentos y agua contaminada.
Los seres humanos se infectan por la ingestión de ooquistes C. parvum que contienen muchos esporozoitos. Los esporozoítos se liberan en el tracto gastrointestinal superior y se unen a las células de la mucosa intestinal, donde se dividen para producir merozoitos. Los merozoitos invaden otras células de la mucosa y se multiplican asexualmente. Algunos de los merozoitos se diferencian en gametocitos masculinos y femeninos y forman un ooquistes en el que se multiplican y se diferencian en esporozoitos. El ooquiste maduro se excreta con la materia fecal e infecta a otros individuos.
CLÍNICA.
Asintomatica. Diarrea aguda autolimitada (inmunocompetentes) o cronica en ocaciones con compromiso vital (inmunodeficientes). Localizacion extraintestinal, en ocasiones, especialmente en pacientes inmunodeficientes, que puede ocasionar colecistitis alitiasica, colangitis, pancreatitis, hepatitis.
DIAGNÓSTICO.
Identificación de los quistes del parasito en las heces. Técnicas de concentración. Tinción de Kinyoun. Detección de antígeno en heces. Visualización de ooquistes en biopsia yeyunal.
TRATAMIENTO.
Autolimitada en inmunocompetentes, no requiere tratamiento. Inmunodeprimidos: correccion de la inmunodeficiencia. El tratamiento especifico no elimina la infeccion, pero reduce la gravedad del cuadro. Nitazoxamida y Paramomicina.
Alternativas: en los casos cronicos rebeldes al tratamiento son importantes las medidas de rehidratacion y tratamiento sintomatico con antiperistalticos y analogos de la somatostatina.
ISOSPORIASIS
Isospora belli
I. belli es protozoo que afecta al intestino delgado. Es cosmopolita y las personas se infectan al ingerir agua o alimentos contaminados con ooquistes maduros.
Tiene una capacidad invasiva. Es una infección poco común de los humanos sana, a pesar de que está siendo visto en número creciente en pacientes con SIDA. La infección se produce por vía oro-fecal. La etapa infecciosa del organismo es un oocisto ovalada que, después de la ingestión, sigue el mismo curso que C. parvum. En individuos normales, infecciones leves se resuelven con reposo y dieta suave y las infecciones más graves pueden ser tratados con medicamentos sulfa. El tratamiento puede tener que ser llevado a cabo durante un período prolongado en pacientes con SIDA.
CLÍNICA.
Asintomatica. Diarrea, flatulencia, colico abdominal, anorexia, febrícula, pérdida de peso. Puede producir eosinofilia periferica. En personas inmunocompetentes suele producir una enfermedad autolimitada. En inmunodeprimidos se cronifica.
DIAGNÓSTICO.
Identificacion del parasito en las heces. Tinciones de Kinyoun.
TRATAMIENTO.
Trimetoprim-Sulfametoxazol (TMS).
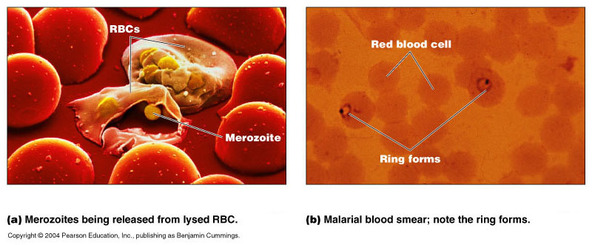
MALARIA
Philum: Apicomplexa
Clase: Aconoidasida
Orden: Haemosporida
Género: Plasmodium
ETIOLOGÍA
Cuatro especies de Plasmodium: P. falciparum, P. vivax, P. ovale y P. malariae.
EPIDEMIOLOGÍA
P. falciparum (malaria terciana maligna) y P. malariae (malaria cuartana) son las especies más comunes del parásito y se encuentran en Asia y África. P. vivax (malaria terciana benigna) predomina en América Latina, la India y Pakistán, mientras que, P. ovale (malaria terciana ovale) se encuentra casi exclusivamente en África.
MORFOLOGÍA
Los trofozoítos son generalmente en forma de anillo, de 1-2µm de tamaño. Las formas sexuales del parásito (gametocitos) son mucho más grandes de 7-14 µm en tamaño. P. falciparum es el más grande y está en forma de banano, mientras que otros son más pequeños y redondos. P. vivax causa el punteado de las células rojas infectadas.
CICLO DE VIDA
Los parásitos de la malaria se transmiten por el mosquito anófeles hembra infectado que inyecta los esporozoitos presentes en la saliva del insecto. Los esporozoitos infectan las células del parénquima hepático, donde pueden permanecer latentes o someterse a las etapas de la esquizogonia para producir esquizontes y merogonia para producir merozoitos (merontes). Cuando las células del parénquima se rompen, miles de merontes se liberan en la sangre e infectan los glóbulos rojos. P. ovale y P. vivax infectan los glóbulos rojos inmaduros mientras que P. malariae infecta las células rojos maduros. P. falciparum infecta ambos. En los glóbulos rojos, los parásitos maduran en trofozoítos. Estos trofozoítos se someten esquizogonia y merogonia en los glóbulos rojos que finalmente estallan y liberan merozoitos hijas. Algunos de los merozoitos se transforman en gametocitos masculinos y femeninos, mientras que otros entran en otras células rojas para continuar el ciclo eritrocítica. Los gametocitos son ingeridos por el mosquito hembra, el macrogameto (gametocito fémina) se transforma en oocineto, es fertilizado, y forma ooquistes en el intestino. El ooquiste produce esporozoitos (esporogonio) que migran a la glándula salival y están listos para infectar a otro huésped.
La malaria se puede transmitir por transfusión y por vía transplacentaria. En esta parasitosis el hombre es el huésped intermediario y el Anopheles el huésped definitivo.
SÍNTOMAS
La sintomatología de la malaria depende de la parasitemia, la presencia del organismo en diferentes órganos y de la carga parasitaria. El período de incubación varía generalmente entre 10 a 30 días. A medida que la carga de parásitos se vuelve significativa, el paciente desarrolla dolor de cabeza, cansancio, dolores vagos en los huesos y articulaciones, las sensaciones de frío y fiebre. A medida que la enfermedad progresa, los escalofríos y la fiebre se vuelven más prominentes. El frío y la fiebre siguen un patrón cíclico (paroxismo) con el período sintomático que dura 8-12 horas. Entre los períodos sintomáticos, hay un período de relativa normalidad, cuya duración depende de la especie del parásito infectante. Este intervalo es de alrededor de 34 a 36 horas en el caso de P. vivax y P. ovale (malaria terciana), y 58 a 60 horas en el caso de P. malariae (malaria cuartana).
Sin tratamiento, todas las especies de malaria humana pueden en última instancia resultar en curación espontánea, excepto con P. falciparum que se hace progresivamente más grave y resulta en la muerte. Este organismo causa el secuestro de la vasculatura capilar en el cerebro, gastrointestinal y los tejidos renales. La malaria crónica resulta en la esplenomegalia, hepatomegalia y síndromes nefríticos.
DIAGNÓSTICO
El diagnóstico se basa en los síntomas y la detección del parásito en frotis sanguíneas con tinción de Giemsa. También hay pruebas bioquímicos para detectar anticuerpos específicos.
TRATAMIENTO Y CONTROL
El tratamiento es eficaz con los diversos derivados de quinina (sulfato de quinina, cloroquina, meflaquina y primaquina, etc.). La resistencia a fármacos, en particular en P. falciparum y en cierta medida en P. vivax es un problema importante.
Las medidas de control son la erradicación de mosquitos anofeles infectados. Prevenir picaduras y hacer vigilancia.
Philum: Apicomplexa
Clase: Aconoidasida
Orden: Haemosporida
Género: Plasmodium
ETIOLOGÍA
Cuatro especies de Plasmodium: P. falciparum, P. vivax, P. ovale y P. malariae.
EPIDEMIOLOGÍA
P. falciparum (malaria terciana maligna) y P. malariae (malaria cuartana) son las especies más comunes del parásito y se encuentran en Asia y África. P. vivax (malaria terciana benigna) predomina en América Latina, la India y Pakistán, mientras que, P. ovale (malaria terciana ovale) se encuentra casi exclusivamente en África.
MORFOLOGÍA
Los trofozoítos son generalmente en forma de anillo, de 1-2µm de tamaño. Las formas sexuales del parásito (gametocitos) son mucho más grandes de 7-14 µm en tamaño. P. falciparum es el más grande y está en forma de banano, mientras que otros son más pequeños y redondos. P. vivax causa el punteado de las células rojas infectadas.
CICLO DE VIDA
Los parásitos de la malaria se transmiten por el mosquito anófeles hembra infectado que inyecta los esporozoitos presentes en la saliva del insecto. Los esporozoitos infectan las células del parénquima hepático, donde pueden permanecer latentes o someterse a las etapas de la esquizogonia para producir esquizontes y merogonia para producir merozoitos (merontes). Cuando las células del parénquima se rompen, miles de merontes se liberan en la sangre e infectan los glóbulos rojos. P. ovale y P. vivax infectan los glóbulos rojos inmaduros mientras que P. malariae infecta las células rojos maduros. P. falciparum infecta ambos. En los glóbulos rojos, los parásitos maduran en trofozoítos. Estos trofozoítos se someten esquizogonia y merogonia en los glóbulos rojos que finalmente estallan y liberan merozoitos hijas. Algunos de los merozoitos se transforman en gametocitos masculinos y femeninos, mientras que otros entran en otras células rojas para continuar el ciclo eritrocítica. Los gametocitos son ingeridos por el mosquito hembra, el macrogameto (gametocito fémina) se transforma en oocineto, es fertilizado, y forma ooquistes en el intestino. El ooquiste produce esporozoitos (esporogonio) que migran a la glándula salival y están listos para infectar a otro huésped.
La malaria se puede transmitir por transfusión y por vía transplacentaria. En esta parasitosis el hombre es el huésped intermediario y el Anopheles el huésped definitivo.
SÍNTOMAS
La sintomatología de la malaria depende de la parasitemia, la presencia del organismo en diferentes órganos y de la carga parasitaria. El período de incubación varía generalmente entre 10 a 30 días. A medida que la carga de parásitos se vuelve significativa, el paciente desarrolla dolor de cabeza, cansancio, dolores vagos en los huesos y articulaciones, las sensaciones de frío y fiebre. A medida que la enfermedad progresa, los escalofríos y la fiebre se vuelven más prominentes. El frío y la fiebre siguen un patrón cíclico (paroxismo) con el período sintomático que dura 8-12 horas. Entre los períodos sintomáticos, hay un período de relativa normalidad, cuya duración depende de la especie del parásito infectante. Este intervalo es de alrededor de 34 a 36 horas en el caso de P. vivax y P. ovale (malaria terciana), y 58 a 60 horas en el caso de P. malariae (malaria cuartana).
Sin tratamiento, todas las especies de malaria humana pueden en última instancia resultar en curación espontánea, excepto con P. falciparum que se hace progresivamente más grave y resulta en la muerte. Este organismo causa el secuestro de la vasculatura capilar en el cerebro, gastrointestinal y los tejidos renales. La malaria crónica resulta en la esplenomegalia, hepatomegalia y síndromes nefríticos.
DIAGNÓSTICO
El diagnóstico se basa en los síntomas y la detección del parásito en frotis sanguíneas con tinción de Giemsa. También hay pruebas bioquímicos para detectar anticuerpos específicos.
TRATAMIENTO Y CONTROL
El tratamiento es eficaz con los diversos derivados de quinina (sulfato de quinina, cloroquina, meflaquina y primaquina, etc.). La resistencia a fármacos, en particular en P. falciparum y en cierta medida en P. vivax es un problema importante.
Las medidas de control son la erradicación de mosquitos anofeles infectados. Prevenir picaduras y hacer vigilancia.
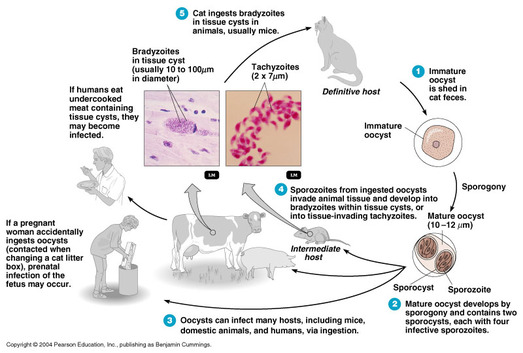
TOXOPLASMOSIS
Toxoplasma gondii
EPIDEMIOLOGÍA
Toxoplasma tiene distribución mundial y el 20% -75% de la población es seropositiva sin ningún episodio sintomático. Sin embargo, la infección representa una grave amenaza en individuos inmunodeprimidos y mujeres embarazadas.
MORFOLOGÍA
Los parásitos intracelulares (taquizoitos) son 3×6µm, en forma de pera que se envuelven en una membrana del parásito para formar un quiste que mide 10-100µm de tamaño. Los quistes en las heces de gato (ooquistes) son 10-13µm de diámetro.
CICLO DE VIDA
El ciclo de vida natural de T. gondii se produce en los gatos y pequeños roedores, aunque el parásito puede crecer en los órganos (cerebro, ojo, el músculo esquelético, etc.) de cualquier mamífero. Los gatos se infectan por la ingestión de quistes en la carne. La eclosión se produce en el intestino delgado, y los microorganismos penetran en las células epiteliales de la submucosa donde se someten a varias generaciones de mitosis, resultando finalmente en el desarrollo de micro (macho) y macro (hembra) gametocitos. macrogametocitos fertilizados se desarrollan en ooquistes que están dados de alta en la luz intestinal y excretados. Los ooquistes se esporulan en el entorno cálido y son infecciosos a una variedad de animales, incluyendo roedores y el hombre. Los esporozoitos liberados de los ooquistes en el intestino delgado penetran la mucosa intestinal y encuentran su camino hacia los macrófagos en los que se dividen muy rápidamente y forman un quiste que puede ocupar toda la célula. Las células infectadas finalmente estallan y liberan los taquizoítos para entrar en otras células, incluyendo las células musculares y nerviosas, donde son protegidos del sistema inmune del huésped y se multiplican lentamente (bradizoítos). Estos quistes son infecciosos para los carnívoros (incluido el hombre).
SÍNTOMAS
Aunque la infección por Toxoplasma es común, rara vez produce síntomas en individuos sanos. Sus graves consecuencias se limitan a las mujeres embarazadas y los huéspedes inmunodeficientes. Las infecciones congénitas ocurren en aproximadamente 1-5 por cada 1000 embarazos de los cuales 5-10% resulta en aborto involuntario y 8-10% en el daño cerebral y ocular grave para el feto. Aunque 58-70% de las mujeres infectadas dará a luz a un hijo normal, una pequeña proporción de bebés desarrollará retino-corditis activa o retraso mental en la niñez o en la edad adulta joven. En los adultos inmunocompetentes, la toxoplasmosis, pueden producir síntomas similares a la gripe, a veces asociados con linfadenopatía. En individuos inmunocomprometidos, la infección resulta en la parasitemia y tiene implicación en el cerebro, pulmón, hígado y otros órganos, y muchas veces la resulta en la muerte.
DIAGNÓSTICO
Observación del parásito en sangre y cortes histológicos. Aislamiento del parásito por inoculación a ratones y cultivo de tejidos. Serológico: anticuerpos específicos. PCR
TRATAMIENTO
Las infecciones agudas se benefician de pirimetamina y ademas sulfadiazina. La espiramicina es una alternativa exitosa.
Toxoplasma gondii
EPIDEMIOLOGÍA
Toxoplasma tiene distribución mundial y el 20% -75% de la población es seropositiva sin ningún episodio sintomático. Sin embargo, la infección representa una grave amenaza en individuos inmunodeprimidos y mujeres embarazadas.
MORFOLOGÍA
Los parásitos intracelulares (taquizoitos) son 3×6µm, en forma de pera que se envuelven en una membrana del parásito para formar un quiste que mide 10-100µm de tamaño. Los quistes en las heces de gato (ooquistes) son 10-13µm de diámetro.
CICLO DE VIDA
El ciclo de vida natural de T. gondii se produce en los gatos y pequeños roedores, aunque el parásito puede crecer en los órganos (cerebro, ojo, el músculo esquelético, etc.) de cualquier mamífero. Los gatos se infectan por la ingestión de quistes en la carne. La eclosión se produce en el intestino delgado, y los microorganismos penetran en las células epiteliales de la submucosa donde se someten a varias generaciones de mitosis, resultando finalmente en el desarrollo de micro (macho) y macro (hembra) gametocitos. macrogametocitos fertilizados se desarrollan en ooquistes que están dados de alta en la luz intestinal y excretados. Los ooquistes se esporulan en el entorno cálido y son infecciosos a una variedad de animales, incluyendo roedores y el hombre. Los esporozoitos liberados de los ooquistes en el intestino delgado penetran la mucosa intestinal y encuentran su camino hacia los macrófagos en los que se dividen muy rápidamente y forman un quiste que puede ocupar toda la célula. Las células infectadas finalmente estallan y liberan los taquizoítos para entrar en otras células, incluyendo las células musculares y nerviosas, donde son protegidos del sistema inmune del huésped y se multiplican lentamente (bradizoítos). Estos quistes son infecciosos para los carnívoros (incluido el hombre).
SÍNTOMAS
Aunque la infección por Toxoplasma es común, rara vez produce síntomas en individuos sanos. Sus graves consecuencias se limitan a las mujeres embarazadas y los huéspedes inmunodeficientes. Las infecciones congénitas ocurren en aproximadamente 1-5 por cada 1000 embarazos de los cuales 5-10% resulta en aborto involuntario y 8-10% en el daño cerebral y ocular grave para el feto. Aunque 58-70% de las mujeres infectadas dará a luz a un hijo normal, una pequeña proporción de bebés desarrollará retino-corditis activa o retraso mental en la niñez o en la edad adulta joven. En los adultos inmunocompetentes, la toxoplasmosis, pueden producir síntomas similares a la gripe, a veces asociados con linfadenopatía. En individuos inmunocomprometidos, la infección resulta en la parasitemia y tiene implicación en el cerebro, pulmón, hígado y otros órganos, y muchas veces la resulta en la muerte.
DIAGNÓSTICO
Observación del parásito en sangre y cortes histológicos. Aislamiento del parásito por inoculación a ratones y cultivo de tejidos. Serológico: anticuerpos específicos. PCR
TRATAMIENTO
Las infecciones agudas se benefician de pirimetamina y ademas sulfadiazina. La espiramicina es una alternativa exitosa.