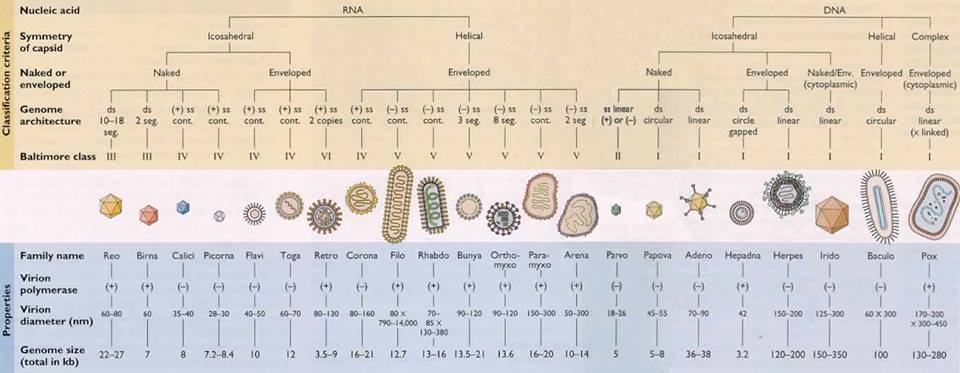
El virus es un agente genético que posee una región central de ácido nucleico, adn o adn (genoma) y que está rodeado por una cubierta de proteina o cápside y, en algunos casos, por una envoltura lipoproteica. Los virus contienen toda la información necesaria para su ciclo reproductor; que solamente puede ocurrir adentro de las células vivas, apoderándose de las enzimas y de la maquinaria biosintética de sus hospedadores.
Los virus difieren entre sí por el tamaño, la forma y la composición química de su genoma. El ciclo vital de los virus consta de las siguientes 4 fases: entrada en la célula, eclipse, multiplicación y liberación del virus.
ADENOVIRUS

Existen adenovirus en todas las partes del mundo. Están presentes durante todo el año y por lo general no producen brotes epidémicos de la enfermedad en la población, los serotipos más frecuentes en las muestras clínicas son los tipos respiratorios de números bajos (1, 2, 3, 5 y 7) y los de tipo de gastroenteritis (40, 41). Los adenovirus se diseminan por el contacto directo, por la vía fecal-oral, por las gotículas respiratorias o por los fómites contaminados.
Los adenovirus se pueden replicar y producir enfermedad en los aparatos respiratorio, digestivo y urinario, así como en el ojo. Muchas infecciones por adenovirus son leves y el virus puede persistir en el huésped durante meses. El nombre “adenovirus” refleja la recuperación de la cepa inicial a partir de explantes de adenoides de seres humanos.
PROPIEDADES IMPORTANTES DE LOS ADENOVIRUS
INFECCIONES POR ADENOVIRUS EN SERES HUMANOS
Los adenovirus intervienen en casi 5% de las enfermedades respiratorias agudas en niños pequeños, pero contribuyen a mucho menos en los adultos. Casi todas las infecciones son leves y ceden espontáneamente. Los virus en ocasiones son causa de enfermedad en otros órganos, sobre todo en los ojos y en el aparato digestivo.
ENFERMEDADES RESPIRATORIAS
Los síntomas característicos consisten en tos, congestión nasal, fiebre y disfagia. Este síndrome suele manifestarse en los lactantes y niños. Por lo general se debe a virus del grupo C. Estos casos son difíciles de distinguir de otras infecciones respiratorias leves por virus que pueden producir síntomas similares.
Se piensa que los adenovirus, sobre todo los tipos 3, 7 y 21, son causa de casi 10 a 20% de las neumonías en la infancia. Se ha comunicado que la neumonía por adenovirus tiene una tasa de mortalidad de 8 a 10% en los niños muy pequeños.
En el año 2007 se presentó un brote de enfermedad respiratoria grave, que algunas veces fue mortal, por una nueva variante del adenovirus 14. Los pacientes afectados eran de todas las edades y comprendían adultos jóvenes sanos.
INFECCIONES OCULARES
La afectación ocular leve puede ser parte de los síndromes respiratorios-faríngeos causados por los adenovirus. La fiebre faringoconjuntival tiende a presentarse en brotes epidémicos, como los que ocurren en campos de verano de los niños (“conjuntivitis de la alberca”) y están relacionados con los adenovirus tipos 3 y 7. La duración de la conjuntivitis es de una a dos semanas y el resultado frecuente es el restablecimiento completo sin ninguna secuela duradera.
INFECCIONES DIGESTIVAS
Muchos adenovirus se replican en las células intestinales y se identifican en las heces, pero la presencia de casi todos los serotipos no se relaciona con enfermedad digestiva. Sin embargo, dos serotipos (tipos 40 y 41) se han vinculado etiológicamente con la gastroenteritis infantil y pueden ser causa de 5 a 15% de los casos de gastroenteritis viral en niños pequeños. Los adenovirus tipos 40 y 41 están presentes en abundancia en las heces diarreicas. Los adenovirus intestinales son muy difíciles de cultivar.
OTRAS ENFERMEDADES
Los pacientes inmunodeprimidos pueden padecer diversas infecciones por adenovirus casuales y graves. El problema más frecuente causado por la infección por adenovirus en pacientes sometidos a trasplante son las enfermedades respiratorias que pueden evolucionar a neumonía grave y pueden ser mortales (por lo general tipos 1 a 7). Los niños que reciben trasplantes hepáticos pueden desarrollar hepatitis por adenovirus en el aloinjerto. Además, los niños con trasplantes cardiacos que presentan infecciones miocárdicas por adenovirus tienen un mayor riesgo de pérdida del injerto.
Los pacientes con síndrome de inmunodeficiencia adquirida (SIDA) pueden padecer infecciones por adenovirus, sobre todo en el tubo digestivo. Es posible que los tipos 11 y 21 provoquen cistitis hemorrágica aguda en los niños, sobre todo en los varones. Los virus suelen detectarse en la orina de estos pacientes.
DIAGNÓSTICO DE LABORATORIO
Detección, aislamiento e identificación del virus. Deben obtenerse muestras de los lugares afectados en las primeras etapas de la enfermedad para optimizar el aislamiento del virus. Dependiendo de la enfermedad clínica, se puede obtener el virus de las heces o de la orina o de un exudado faríngeo, conjuntival, o rectal.
Se pueden identificar cepas como adenovirus mediante las pruebas inmunofluorescentes en las que se utiliza anticuerpo antihexona en células infectadas. Las pruebas miden antígenos específicos y se pueden utilizar para identificar serotipos específicos.
La detección de adenovirus infecciosos puede realizarse rápidamente utilizando la técnica centrifugación y cultivo. Se centrifugan especímenes virales directamente en células de cultivo de tejido; se incuban durante uno a dos días y luego se realizan pruebas con anticuerpos monoclonales dirigidos contra un epitopo reactivo de grupo en el antígeno de hexona.
Se pueden utilizar los análisis de reacción en cadena de la polimerasa (PCR) para el diagnóstico de infecciones por adenovirus en muestras de tejido o líquidos corporales.
Estudio serológico. La prueba CF (fijador del complemento) es un método fácilmente aplicado para detectar la infección por cualquier miembro del grupo de los adenovirus, aunque la prueba tiene una baja sensibilidad.
TRATAMIENTO
No se dispone de ningún tratamiento específico para las infecciones por adenovirus.
Los adenovirus se pueden replicar y producir enfermedad en los aparatos respiratorio, digestivo y urinario, así como en el ojo. Muchas infecciones por adenovirus son leves y el virus puede persistir en el huésped durante meses. El nombre “adenovirus” refleja la recuperación de la cepa inicial a partir de explantes de adenoides de seres humanos.
PROPIEDADES IMPORTANTES DE LOS ADENOVIRUS
- Virión: Icosaédrico de 70 a 90nm de diámetro, 252 capsómeros; la fibra se proyecta desde cada vértice
- Genoma: DNA bicatenario, lineal, infeccioso
- Envoltura: Ninguna
- Replicación: Núcleo
- Características sobresalientes: Modelos excelentes para estudios moleculares de procesos de células eucariotas
INFECCIONES POR ADENOVIRUS EN SERES HUMANOS
Los adenovirus intervienen en casi 5% de las enfermedades respiratorias agudas en niños pequeños, pero contribuyen a mucho menos en los adultos. Casi todas las infecciones son leves y ceden espontáneamente. Los virus en ocasiones son causa de enfermedad en otros órganos, sobre todo en los ojos y en el aparato digestivo.
ENFERMEDADES RESPIRATORIAS
Los síntomas característicos consisten en tos, congestión nasal, fiebre y disfagia. Este síndrome suele manifestarse en los lactantes y niños. Por lo general se debe a virus del grupo C. Estos casos son difíciles de distinguir de otras infecciones respiratorias leves por virus que pueden producir síntomas similares.
Se piensa que los adenovirus, sobre todo los tipos 3, 7 y 21, son causa de casi 10 a 20% de las neumonías en la infancia. Se ha comunicado que la neumonía por adenovirus tiene una tasa de mortalidad de 8 a 10% en los niños muy pequeños.
En el año 2007 se presentó un brote de enfermedad respiratoria grave, que algunas veces fue mortal, por una nueva variante del adenovirus 14. Los pacientes afectados eran de todas las edades y comprendían adultos jóvenes sanos.
INFECCIONES OCULARES
La afectación ocular leve puede ser parte de los síndromes respiratorios-faríngeos causados por los adenovirus. La fiebre faringoconjuntival tiende a presentarse en brotes epidémicos, como los que ocurren en campos de verano de los niños (“conjuntivitis de la alberca”) y están relacionados con los adenovirus tipos 3 y 7. La duración de la conjuntivitis es de una a dos semanas y el resultado frecuente es el restablecimiento completo sin ninguna secuela duradera.
INFECCIONES DIGESTIVAS
Muchos adenovirus se replican en las células intestinales y se identifican en las heces, pero la presencia de casi todos los serotipos no se relaciona con enfermedad digestiva. Sin embargo, dos serotipos (tipos 40 y 41) se han vinculado etiológicamente con la gastroenteritis infantil y pueden ser causa de 5 a 15% de los casos de gastroenteritis viral en niños pequeños. Los adenovirus tipos 40 y 41 están presentes en abundancia en las heces diarreicas. Los adenovirus intestinales son muy difíciles de cultivar.
OTRAS ENFERMEDADES
Los pacientes inmunodeprimidos pueden padecer diversas infecciones por adenovirus casuales y graves. El problema más frecuente causado por la infección por adenovirus en pacientes sometidos a trasplante son las enfermedades respiratorias que pueden evolucionar a neumonía grave y pueden ser mortales (por lo general tipos 1 a 7). Los niños que reciben trasplantes hepáticos pueden desarrollar hepatitis por adenovirus en el aloinjerto. Además, los niños con trasplantes cardiacos que presentan infecciones miocárdicas por adenovirus tienen un mayor riesgo de pérdida del injerto.
Los pacientes con síndrome de inmunodeficiencia adquirida (SIDA) pueden padecer infecciones por adenovirus, sobre todo en el tubo digestivo. Es posible que los tipos 11 y 21 provoquen cistitis hemorrágica aguda en los niños, sobre todo en los varones. Los virus suelen detectarse en la orina de estos pacientes.
DIAGNÓSTICO DE LABORATORIO
Detección, aislamiento e identificación del virus. Deben obtenerse muestras de los lugares afectados en las primeras etapas de la enfermedad para optimizar el aislamiento del virus. Dependiendo de la enfermedad clínica, se puede obtener el virus de las heces o de la orina o de un exudado faríngeo, conjuntival, o rectal.
Se pueden identificar cepas como adenovirus mediante las pruebas inmunofluorescentes en las que se utiliza anticuerpo antihexona en células infectadas. Las pruebas miden antígenos específicos y se pueden utilizar para identificar serotipos específicos.
La detección de adenovirus infecciosos puede realizarse rápidamente utilizando la técnica centrifugación y cultivo. Se centrifugan especímenes virales directamente en células de cultivo de tejido; se incuban durante uno a dos días y luego se realizan pruebas con anticuerpos monoclonales dirigidos contra un epitopo reactivo de grupo en el antígeno de hexona.
Se pueden utilizar los análisis de reacción en cadena de la polimerasa (PCR) para el diagnóstico de infecciones por adenovirus en muestras de tejido o líquidos corporales.
Estudio serológico. La prueba CF (fijador del complemento) es un método fácilmente aplicado para detectar la infección por cualquier miembro del grupo de los adenovirus, aunque la prueba tiene una baja sensibilidad.
TRATAMIENTO
No se dispone de ningún tratamiento específico para las infecciones por adenovirus.
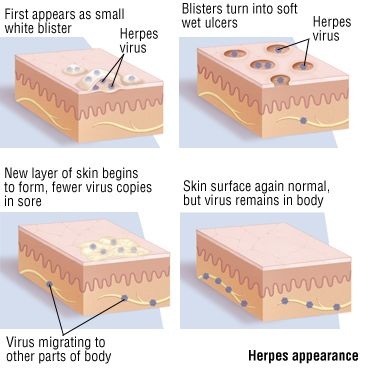
HERPESVIRUS
La familia de los herpesvirus contiene varios de los virus patógenos humanos más importantes. Los herpesvirus producen una amplia gama de enfermedades clínicas. Desde el punto de vista clínico, la infección reactivada pueda ser muy diferente a la enfermedad causada por la infección primaria. Los herpesvirus que suelen infectar al ser humano son el virus del herpes simple tipos 1 y 2 (HSV-1, HSV-2), el virus de la varicela-zoster, el citomegalovirus, el virus de Epstein-Barr (EBV), los herpesvirus 6 y 7, el herpesvirus 8 (herpesvirus relacionado con el sarcoma de Kaposi.
PROPIEDADES IMPORTANTES DE LOS HERPESVIRUS
INFECCIONES POR HERPESVIRUS EN SERES HUMANOS
HERPES SIMPLE TIPOS 1 Y 2
La infección por VHS-1 es frecuente en sitios hacinados y con condiciones precarias de higiene. La infección por VHS-2 depende de la actividad sexual. La infección por VHS-1 puede originar cuadros clínicos de variada severidad, que oscilan desde la gingovoestomatitis, herpes labial, panadizo herpético, meningitis, encefalitis con alta mortalidad y queratitis herpética que a su vez puede originar ceguera. El VHS-1 en ubicación oral se transmite por saliva, besos, por compartir vasos, cepillos de dientes y en otras partes del cuerpo se debe a contacto del virus con la piel, se autotransmite con frecuencia, principalmente a los ojos. El VHS-2 se transmite por secreciones vaginales, contacto sexual y al neonato durante el paso por el canal de parto infectado.
El herpes genital activo en la madre es un factor obvio de riesgo aunque en gran porcentaje de los niños infectados la causa es herpes asintomático.
La posibilidad de que VHS-1 y VHS-2 establezcan infecciones latentes con recidivas asintomáticas favorece su transmisión, ya que un individuo infectado puede ser transmisor durante toda su vida. Los virus infectantes se encuentran en el líquido de las vesículas.
DIAGNÓSTICO
El diagnóstico de laboratorio económico y rápido se realiza mediante la prueba de Tzank que consiste en hacer una impronta de las células y teñirlas con el colorante de Wright o Giemsa, y observar células fusionadas con varios núcleos, sincitios, así como inclusiones nucleares de Cowdry. No es posible confirmar la presencia del virus por medio de esta técnica ya que otros virus producen el mismo efecto en las células, inclusive el VVZ. Actualmente se hace uso de técnicas inmunoenzimáticas, biológicas, bioquímicas y de biología molecular para detectar anticuerpos o antígenos virales. La detección de anticuerpos solo es de utilidad para detección de la primo infección y estudios epidemiológicos.
TRATAMIENTO
Existen antivirales efectivos utilizados en el tratamiento de infecciones por VHS-1 y VHS-2, entre ellos famciclovir, aciclovir, valaciclovir. Los antivirales no eliminan las partículas virales que se encuentran en ganglios neurales, solo impiden su replicación, por lo que pueden presentarse reactivaciones. En estos casos, el uso de dosis mínimas de los fármacos, durante un tiempo prolongado, tratamiento denominado supresivo, se indica en los pacientes con brotes constantes, prolongados o intensos, aunque debe contemplarse la posibilidad de resistencias.
VARICELA ZOSTER
El virus de varicela-zoster es morfológicamente idéntico al HSV. No tiene ningún reservorio animal. El virus se propaga en los cultivos de tejido embrionario humano y produce cuerpos de inclusión intranuclear característicos.
El virus de la varicela (VVZ) origina varicela y su reactivación causa herpes zoster. Se caracteriza por una infección neurológica y dermatológica, posterior a un episodio de varicela en los ganglios sensitivos espinales y craneales.
Herpes zozster se presenta como una erupción con vesículas de topografía unilateral, que usualmente afectan de 1a 3 dermatomas. Dicha reactivación ocurre, por lo general, una vez en la vida, sobre todo en pacientes de la tercera edad o en aquellos inmunodeprimidos. El dolor asociado es permanente durante la fase aguda. Una vez que se han resuelto las vesículas, un gran número de pacientes mantienen dolor persistente, durante meses o años.
Complicaciones. La neuralgia postherpética. En individuos inmunocomprometidos puede dar lugar a enfermedades progresivas y graves, principalmente encefalitis post-infección y neumonía, en algunos casos fatales. La respuesta inmune celular que generalmente es más potente en adultos que en niños causa durante la infección primaria lesiones y cuadros graves, principalmente en pulmones, y da lugar a 20-30% de los pacientes con neumonía intersticial.
DIAGNÓSTICO
El diagnóstico se basa en la prueba de Tzank, con las dificultades mencionadas; el virus se puede aislar de las vesículas y recientemente se utilizan técnicas de biología molecular para su identificación.
TRATAMIENTO
Aciclovir
VIRUS DE EPSTEIN-BARR
Los síntomas por VEB en los niños son generalmente subclínicos, en cambio en adolescentes origina mononucleosis infecciosa, que se caracteriza por presentar malestar general, faringitis, linfocitosis y frecuentemente hepatoesplenomegalia. Los pacientes se quejan de cansancio. La incidencia de mononucleosis infecciosa a nivel mundial se aproxima al 100%. La enfermedad recurrente es una fuente de contagio y puede causar diseminación asintomática.
VEB infecta las células epiteliales de la cavidad oral donde se multiplica, pasa a la saliva y se disemina al tejido linfático, es mitógeno para las células B y permanece en ellas en forma latente. La inmunidad celular permanente participa en el control de la infección.
Complicaciones. Puede originar trastornos neurológicos como meningoencefalitis, síndrome de Guillian Barré. Se le ha asociado con carcinoma nasofaríngeo y con linfoma de Burkitt.
DIAGNÓSTICO
El diagnóstico de laboratorio se hace frecuentemente por linfocitos atípicos y anticuerpos heterofílicos.
TRATAMIENTO
No se tiene tratamiento efectivo, la enfermedad es ubicua.
Se transmite por la vía respiratoria, por gotitas, en los adolescentes a través de besos y contactos de saliva. La mejor forma de prevenir la mononucleosis infecciosa es exponerse al virus en la niñez ya que la enfermedad es muy benigna a edades tempranas.
CITOMEGALOVIRUS
Los citomegalovirus (CMV) son herpesvirus ubicuos que son causas frecuentes de enfermedad humana. Los citomegalovirus son los agentes de la infección congénita más frecuente.
La citomegalia es una infección generalizada en los lactantes causada por una infección intrauterina o posnatal inicial por los CMV. Este virus plantea un problema de salud pública importante debido a su alta frecuencia de infecciones congénitas, que pueden desencadenar anomalías congénitas graves. La infección no manifiesta es frecuente durante la infancia y la adolescencia. A menudo se detectan infecciones graves por CMV en adultos inmunodeprimidos.
CMV tiene el máximo contenido genético de los herpesvirus humanos. Su genoma de DNA es significativamente mayor que el de HSV. Una de sus glucoproteína de la superficie celular, actúa como un receptor de Fc que de manera inespecífica se une a la porción Fc de las inmunoglobulinas. Esto puede ayudar a las células infectadas a evadir la eliminación inmunitaria al proporcionar una cubierta protectora de inmunoglobulinas irrelevantes del hospedador.
El CMV humano se replica invitro sólo en fibroblastos humanos, aunque el virus suele aislarse de células epiteliales del hospedador. CMV produce un efecto citopático característico. Se forman inclusiones citoplásmicas perinucleares además de las inclusiones intranucleares características de los herpesvirus. Se observan células multinucleadas. Muchas células afectadas adquieren un gran tamaño. Las células citomegálicas que tienen inclusiones pueden detectarse en muestras de personas infectadas.
DIAGNÓSTICO
Se hace por la presencia de células citomegálicas, que son de gran tamaño y presentan una inclusión intranuclear basófila densa, ojo de lechuza. Las células citomegalicas se encuentran en cualquier tejido del cuerpo y en la orina; las inclusiones se observan fácilmente con tinción de Papanicolaou, hematoxilina y eosina.
TRATAMIENTO, TRANSMISIÓN PREVENCIÓN Y CONTROL
No se dispone de fármacos específicos, se utilizan los mencionados para las otras infecciones herpéticas, principalmente el ganciclovir.
Se transmite en transfusiones de sangre y en transplantes de órganos. Las infecciones en estas intervenciones son generalmente asintomáticas, y en caso de existir, los signos y síntomas son similares a los de mononucleosis infecciosa. El virus se encuentra con frecuencia en el riñón donde se replica y se elimina por la orina, lo cual facilita su aislamiento.
PROPIEDADES IMPORTANTES DE LOS HERPESVIRUS
- Virión: esférico, 150 a 200nm de diámetro (icosaédrico)
- Genoma: DNA bicatenario, lineal
- Envoltura: contiene glucoproteínas virales
- Replicación: núcleo, gemación a partir de la membrana nuclear
- Características sobresalientes: Codifica muchas enzimas. Establece infecciones latentes. Persiste en forma indefinida en hospedadores infectados. Se reactiva con frecuencia en hospedadores inmunodeprimidos. Algunos provocan cáncer
INFECCIONES POR HERPESVIRUS EN SERES HUMANOS
HERPES SIMPLE TIPOS 1 Y 2
La infección por VHS-1 es frecuente en sitios hacinados y con condiciones precarias de higiene. La infección por VHS-2 depende de la actividad sexual. La infección por VHS-1 puede originar cuadros clínicos de variada severidad, que oscilan desde la gingovoestomatitis, herpes labial, panadizo herpético, meningitis, encefalitis con alta mortalidad y queratitis herpética que a su vez puede originar ceguera. El VHS-1 en ubicación oral se transmite por saliva, besos, por compartir vasos, cepillos de dientes y en otras partes del cuerpo se debe a contacto del virus con la piel, se autotransmite con frecuencia, principalmente a los ojos. El VHS-2 se transmite por secreciones vaginales, contacto sexual y al neonato durante el paso por el canal de parto infectado.
El herpes genital activo en la madre es un factor obvio de riesgo aunque en gran porcentaje de los niños infectados la causa es herpes asintomático.
La posibilidad de que VHS-1 y VHS-2 establezcan infecciones latentes con recidivas asintomáticas favorece su transmisión, ya que un individuo infectado puede ser transmisor durante toda su vida. Los virus infectantes se encuentran en el líquido de las vesículas.
DIAGNÓSTICO
El diagnóstico de laboratorio económico y rápido se realiza mediante la prueba de Tzank que consiste en hacer una impronta de las células y teñirlas con el colorante de Wright o Giemsa, y observar células fusionadas con varios núcleos, sincitios, así como inclusiones nucleares de Cowdry. No es posible confirmar la presencia del virus por medio de esta técnica ya que otros virus producen el mismo efecto en las células, inclusive el VVZ. Actualmente se hace uso de técnicas inmunoenzimáticas, biológicas, bioquímicas y de biología molecular para detectar anticuerpos o antígenos virales. La detección de anticuerpos solo es de utilidad para detección de la primo infección y estudios epidemiológicos.
TRATAMIENTO
Existen antivirales efectivos utilizados en el tratamiento de infecciones por VHS-1 y VHS-2, entre ellos famciclovir, aciclovir, valaciclovir. Los antivirales no eliminan las partículas virales que se encuentran en ganglios neurales, solo impiden su replicación, por lo que pueden presentarse reactivaciones. En estos casos, el uso de dosis mínimas de los fármacos, durante un tiempo prolongado, tratamiento denominado supresivo, se indica en los pacientes con brotes constantes, prolongados o intensos, aunque debe contemplarse la posibilidad de resistencias.
VARICELA ZOSTER
El virus de varicela-zoster es morfológicamente idéntico al HSV. No tiene ningún reservorio animal. El virus se propaga en los cultivos de tejido embrionario humano y produce cuerpos de inclusión intranuclear característicos.
El virus de la varicela (VVZ) origina varicela y su reactivación causa herpes zoster. Se caracteriza por una infección neurológica y dermatológica, posterior a un episodio de varicela en los ganglios sensitivos espinales y craneales.
Herpes zozster se presenta como una erupción con vesículas de topografía unilateral, que usualmente afectan de 1a 3 dermatomas. Dicha reactivación ocurre, por lo general, una vez en la vida, sobre todo en pacientes de la tercera edad o en aquellos inmunodeprimidos. El dolor asociado es permanente durante la fase aguda. Una vez que se han resuelto las vesículas, un gran número de pacientes mantienen dolor persistente, durante meses o años.
Complicaciones. La neuralgia postherpética. En individuos inmunocomprometidos puede dar lugar a enfermedades progresivas y graves, principalmente encefalitis post-infección y neumonía, en algunos casos fatales. La respuesta inmune celular que generalmente es más potente en adultos que en niños causa durante la infección primaria lesiones y cuadros graves, principalmente en pulmones, y da lugar a 20-30% de los pacientes con neumonía intersticial.
DIAGNÓSTICO
El diagnóstico se basa en la prueba de Tzank, con las dificultades mencionadas; el virus se puede aislar de las vesículas y recientemente se utilizan técnicas de biología molecular para su identificación.
TRATAMIENTO
Aciclovir
VIRUS DE EPSTEIN-BARR
Los síntomas por VEB en los niños son generalmente subclínicos, en cambio en adolescentes origina mononucleosis infecciosa, que se caracteriza por presentar malestar general, faringitis, linfocitosis y frecuentemente hepatoesplenomegalia. Los pacientes se quejan de cansancio. La incidencia de mononucleosis infecciosa a nivel mundial se aproxima al 100%. La enfermedad recurrente es una fuente de contagio y puede causar diseminación asintomática.
VEB infecta las células epiteliales de la cavidad oral donde se multiplica, pasa a la saliva y se disemina al tejido linfático, es mitógeno para las células B y permanece en ellas en forma latente. La inmunidad celular permanente participa en el control de la infección.
Complicaciones. Puede originar trastornos neurológicos como meningoencefalitis, síndrome de Guillian Barré. Se le ha asociado con carcinoma nasofaríngeo y con linfoma de Burkitt.
DIAGNÓSTICO
El diagnóstico de laboratorio se hace frecuentemente por linfocitos atípicos y anticuerpos heterofílicos.
TRATAMIENTO
No se tiene tratamiento efectivo, la enfermedad es ubicua.
Se transmite por la vía respiratoria, por gotitas, en los adolescentes a través de besos y contactos de saliva. La mejor forma de prevenir la mononucleosis infecciosa es exponerse al virus en la niñez ya que la enfermedad es muy benigna a edades tempranas.
CITOMEGALOVIRUS
Los citomegalovirus (CMV) son herpesvirus ubicuos que son causas frecuentes de enfermedad humana. Los citomegalovirus son los agentes de la infección congénita más frecuente.
La citomegalia es una infección generalizada en los lactantes causada por una infección intrauterina o posnatal inicial por los CMV. Este virus plantea un problema de salud pública importante debido a su alta frecuencia de infecciones congénitas, que pueden desencadenar anomalías congénitas graves. La infección no manifiesta es frecuente durante la infancia y la adolescencia. A menudo se detectan infecciones graves por CMV en adultos inmunodeprimidos.
CMV tiene el máximo contenido genético de los herpesvirus humanos. Su genoma de DNA es significativamente mayor que el de HSV. Una de sus glucoproteína de la superficie celular, actúa como un receptor de Fc que de manera inespecífica se une a la porción Fc de las inmunoglobulinas. Esto puede ayudar a las células infectadas a evadir la eliminación inmunitaria al proporcionar una cubierta protectora de inmunoglobulinas irrelevantes del hospedador.
El CMV humano se replica invitro sólo en fibroblastos humanos, aunque el virus suele aislarse de células epiteliales del hospedador. CMV produce un efecto citopático característico. Se forman inclusiones citoplásmicas perinucleares además de las inclusiones intranucleares características de los herpesvirus. Se observan células multinucleadas. Muchas células afectadas adquieren un gran tamaño. Las células citomegálicas que tienen inclusiones pueden detectarse en muestras de personas infectadas.
DIAGNÓSTICO
Se hace por la presencia de células citomegálicas, que son de gran tamaño y presentan una inclusión intranuclear basófila densa, ojo de lechuza. Las células citomegalicas se encuentran en cualquier tejido del cuerpo y en la orina; las inclusiones se observan fácilmente con tinción de Papanicolaou, hematoxilina y eosina.
TRATAMIENTO, TRANSMISIÓN PREVENCIÓN Y CONTROL
No se dispone de fármacos específicos, se utilizan los mencionados para las otras infecciones herpéticas, principalmente el ganciclovir.
Se transmite en transfusiones de sangre y en transplantes de órganos. Las infecciones en estas intervenciones son generalmente asintomáticas, y en caso de existir, los signos y síntomas son similares a los de mononucleosis infecciosa. El virus se encuentra con frecuencia en el riñón donde se replica y se elimina por la orina, lo cual facilita su aislamiento.
PICORNAVIRUS (GRUPOS DE ENTEROVIRUS Y RINOVIRUS)
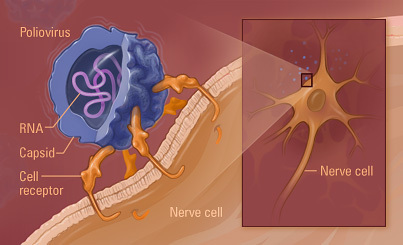
Los enterovirus son residentes transitorios del tubo digestivo humano y pueden aislarse de la faringe o del colon. Los rinovirus se aíslan principalmente de la nariz y la faringe.
PROPIEDADES IMPORTANTES DE LOS PICORNAVIRUS
La poliomielitis es una enfermedad infecciosa aguda que en su forma grave afecta al sistema nervioso central. La destrucción de las motoneuronas en la médula espinal da por resultado parálisis flácida. Sin embargo, la mayor parte de las infecciones por poliovirus es asintomática.
El poliovirus ha servido de picornavirus modelo en muchos estudios de laboratorio de biología molecular de replicación de picornavirus.
MANIFESTACIONES CLÍNICAS
Cuando una persona que es susceptible a la infección se expone al virus, la respuesta varía desde la infección asintomática hasta una enfermedad febril leve y parálisis grave y permanente. La mayor parte de las infecciones es leve; sólo cerca de 1% de las infecciones produce enfermedad clínica.
ENFERMEDAD LEVE
Ésta es la variante más frecuente de la enfermedad. El paciente sólo tiene una enfermedad leve, caracterizada por fiebre, ataque al estado general, somnolencia, cefalea, náusea, vómito, estreñimiento y faringitis en diversas combinaciones. La recuperación ocurre en pocos días.
POLIOMIELITIS NO PARALÍTICA (MENINGITIS ASÉPTICA)
Además de los signos y síntomas de la enfermedad leve, este paciente tiene rigidez y dolor en la espalda y el cuello. La enfermedad dura dos a 10 días y el restablecimiento es rápido y completo. El poliovirus es sólo uno de los múltiples virus que producen meningitis aséptica. En un pequeño porcentaje de los casos, la enfermedad avanza a la parálisis.
POLIOMIELITIS PARALÍTICA
La manifestación predominante es la parálisis flácida resultado de la lesión de la motoneurona inferior. Sin embargo, también se presentan incoordinación secundaria a la invasión del tronco encefálico y espasmos dolorosos de los músculos no paralizados. El grado de lesión es muy variable. El restablecimiento máximo por lo general ocurre en los primeros seis meses y la parálisis residual persiste por mucho más tiempo.
ATROFIA MUSCULAR PROGRESIVA DESPUÉS DE LA POLIOMIELITIS
Se ha observado un recrudecimiento de la parálisis y de la atrofia muscular en los pacientes decenios después de haber sufrido poliomielitis paralítica. Si bien la atrofia muscular progresiva consecutiva a la poliomielitis es poco frecuente, constituye un síndrome específico. No parece ser consecuencia de la infección persistente sino más bien resultado de cambios fisiológicos y seniles en los pacientes con parálisis que ya tienen una pérdida de las funciones neuromusculares.
DIAGNÓSTICO
El virus puede obtenerse de exudados faríngeos obtenidos poco después del inicio de la enfermedad así como de exudados rectales o de muestras de heces obtenidas por periodos prolongados.
No se han identificado portadores permanentes entre las personas inmunocompetentes, pero se ha observado la excreción de poliovirus a largo plazo en algunas personas inmunodeficientes.
Los cultivos de células humanas o de mono se inoculan, incuban y observan. Los efectos citopatógenos aparecen en un lapso de tres a seis días. Se identifica un virus aislado y se tipifica mediante neutralización con antisuero específico. Asimismo, se puede identificar el virus mediante análisis de reacción en cadena de la polimerasa (PCR).
PREVENCIÓN Y CONTROL
Se dispone de vacunas de virus vivos y virus muertos. La vacuna formalinizada (Salk) se prepara a partir de virus desarrollados en cultivos de riñón de mono. La vacuna de virus muertos produce anticuerpos humorales pero no desencadena inmunidad intestinal local de manera que el virus todavía puede multiplicarse en el intestino. Las vacunas orales contienen virus vivos atenuados desarrollados en cultivos primarios de células diploides de monos o seres humanos.
PROPIEDADES IMPORTANTES DE LOS PICORNAVIRUS
- Virión: Icosaédrico, 28 a 30 nm de diámetro, contiene 60 subunidades
- Genoma: RNA monocatenario, lineal, de polaridad positiva, infeccioso
- Proteínas: Cuatro polipéptidos principales desdoblados a partir de una poliproteína precursora de gran tamaño. Las proteínas de la cápside de la superficie VP1 y VP3 son zonas de unión a anticuerpo importantes. VP4 es una proteína interna
- Envoltura: Ninguna
- Replicación: Citoplasma
- Característica sobresaliente: La familia está constituida por muchos tipos de enterovirus y rinovirus que infectan al ser humano y a los animales inferiores, causando diversas enfermedades que van desde la poliomielitis hasta la meningitis aséptica y el resfriado común
La poliomielitis es una enfermedad infecciosa aguda que en su forma grave afecta al sistema nervioso central. La destrucción de las motoneuronas en la médula espinal da por resultado parálisis flácida. Sin embargo, la mayor parte de las infecciones por poliovirus es asintomática.
El poliovirus ha servido de picornavirus modelo en muchos estudios de laboratorio de biología molecular de replicación de picornavirus.
MANIFESTACIONES CLÍNICAS
Cuando una persona que es susceptible a la infección se expone al virus, la respuesta varía desde la infección asintomática hasta una enfermedad febril leve y parálisis grave y permanente. La mayor parte de las infecciones es leve; sólo cerca de 1% de las infecciones produce enfermedad clínica.
ENFERMEDAD LEVE
Ésta es la variante más frecuente de la enfermedad. El paciente sólo tiene una enfermedad leve, caracterizada por fiebre, ataque al estado general, somnolencia, cefalea, náusea, vómito, estreñimiento y faringitis en diversas combinaciones. La recuperación ocurre en pocos días.
POLIOMIELITIS NO PARALÍTICA (MENINGITIS ASÉPTICA)
Además de los signos y síntomas de la enfermedad leve, este paciente tiene rigidez y dolor en la espalda y el cuello. La enfermedad dura dos a 10 días y el restablecimiento es rápido y completo. El poliovirus es sólo uno de los múltiples virus que producen meningitis aséptica. En un pequeño porcentaje de los casos, la enfermedad avanza a la parálisis.
POLIOMIELITIS PARALÍTICA
La manifestación predominante es la parálisis flácida resultado de la lesión de la motoneurona inferior. Sin embargo, también se presentan incoordinación secundaria a la invasión del tronco encefálico y espasmos dolorosos de los músculos no paralizados. El grado de lesión es muy variable. El restablecimiento máximo por lo general ocurre en los primeros seis meses y la parálisis residual persiste por mucho más tiempo.
ATROFIA MUSCULAR PROGRESIVA DESPUÉS DE LA POLIOMIELITIS
Se ha observado un recrudecimiento de la parálisis y de la atrofia muscular en los pacientes decenios después de haber sufrido poliomielitis paralítica. Si bien la atrofia muscular progresiva consecutiva a la poliomielitis es poco frecuente, constituye un síndrome específico. No parece ser consecuencia de la infección persistente sino más bien resultado de cambios fisiológicos y seniles en los pacientes con parálisis que ya tienen una pérdida de las funciones neuromusculares.
DIAGNÓSTICO
El virus puede obtenerse de exudados faríngeos obtenidos poco después del inicio de la enfermedad así como de exudados rectales o de muestras de heces obtenidas por periodos prolongados.
No se han identificado portadores permanentes entre las personas inmunocompetentes, pero se ha observado la excreción de poliovirus a largo plazo en algunas personas inmunodeficientes.
Los cultivos de células humanas o de mono se inoculan, incuban y observan. Los efectos citopatógenos aparecen en un lapso de tres a seis días. Se identifica un virus aislado y se tipifica mediante neutralización con antisuero específico. Asimismo, se puede identificar el virus mediante análisis de reacción en cadena de la polimerasa (PCR).
PREVENCIÓN Y CONTROL
Se dispone de vacunas de virus vivos y virus muertos. La vacuna formalinizada (Salk) se prepara a partir de virus desarrollados en cultivos de riñón de mono. La vacuna de virus muertos produce anticuerpos humorales pero no desencadena inmunidad intestinal local de manera que el virus todavía puede multiplicarse en el intestino. Las vacunas orales contienen virus vivos atenuados desarrollados en cultivos primarios de células diploides de monos o seres humanos.
REOVIRUS
Los reovirus son virus de tamano mediano con un genoma de RNA segmentado bicatenario. La familia comprende rotavirus humano, la causa más importante de la gastroenteritis infantil en todo el mundo.
PROPIEDADES IMPORTANTES DE LOS REOVIRUS
Los rotavirus se parecen a los reovirus por sus características morfológicas y mecanismos de replicación.
PATOGENIA
Los rotavirus infectan las células de las vellosidades del intestino delgado (respetan la mucosa gástrica y la colonica). Se multiplican en el citoplasma de enterocitos y lesionan sus mecanismos de transporte. Las células lesionadas se desprenden hacia la luz del intestino y liberan grandes cantidades de virus, que aparecen en las heces (hasta 1012 partículas por gramo de heces). La excreción viral suele persistir durante 2 a 12 días en pacientes por lo demás sanos pero puede prolongarse en individuos desnutridos. En ocasiones la diarrea por rotavirus se debe a alteraciones de la absorción de sodio y glucosa a medida que las células lesionadas en las vellosidades son remplazadas por células inmaduras de las criptas que no absorben. El establecimiento de la función puede tardar tres a ocho semanas.
MANIFESTACIONES CLÍNICAS Y DIAGNÓSTICO DE LABORATORIO
Hay un periodo de incubación de uno a tres días. Los síntomas característicos consisten en diarrea liquida, fiebre, dolor abdominal y vomito, lo que desencadena deshidratación.
En los lactantes y en los niños, la perdida grave de electrolitos y líquidos puede ser mortal si no se trata. Los pacientes con casos más leves manifiestan síntomas durante tres a ocho días y luego se restablecen por completo. Sin embargo, la excreción viral en las heces puede persistir hasta por 50 días después de iniciada la diarrea. Se presentan infecciones asintomáticas, con seroconversión. En los niños con inmunodeficiencias, el rotavirus puede causar una enfermedad grave y prolongada.
El diagnostico de laboratorio se basa en la demostración del virus en las heces obtenidas en las primeras etapas de la enfermedad y en la elevación del título de anticuerpos. El virus en las heces se demuestra mediante enzimoinmunoanalisis (EIA) o microscopia inmunoelectronica (IEM). La prueba de EIA es más sensible que la de IEM. El método de detección mas sensible es la genotipificacion del acido nucleico del rotavirus obtenido de muestras de heces mediante reacción en cadena de la polimerasa. Se pueden utilizar las pruebas serológicas para detectar una elevación del título de anticuerpo, sobre todo ELISA.
TRATAMIENTO
El tratamiento de la gastroenteritis es sintomático, para corregir la perdida de agua y electrolitos que pueden desencadenar deshidratación, acidosis, choque y muerte del paciente. El tratamiento consiste en la reposición de líquidos y el restablecimiento del equilibrio electrolítico por vía intravenosa o por vía oral, como sea factible.
PROPIEDADES IMPORTANTES DE LOS REOVIRUS
- Virión: Icosaédrico, de 60 a 80 nm de diámetro, doble envoltura de la cápside
- Genoma: RNA bicatenario, lineal, segmentado
- Envoltura: Ninguna (la seudoenvoltura transitoria está presente durante la morfogénesis de la partícula de rotavirus)
- Replicación: Citoplasma; viriones no descubiertos completamente
- Características sobresalientes: El reordenamiento genético ocurre rápidamente. Los rotavirus son la causa principal de diarrea infantil. Los reovirus son buenos modelos de estudios moleculares de la patogenia viral
Los rotavirus se parecen a los reovirus por sus características morfológicas y mecanismos de replicación.
PATOGENIA
Los rotavirus infectan las células de las vellosidades del intestino delgado (respetan la mucosa gástrica y la colonica). Se multiplican en el citoplasma de enterocitos y lesionan sus mecanismos de transporte. Las células lesionadas se desprenden hacia la luz del intestino y liberan grandes cantidades de virus, que aparecen en las heces (hasta 1012 partículas por gramo de heces). La excreción viral suele persistir durante 2 a 12 días en pacientes por lo demás sanos pero puede prolongarse en individuos desnutridos. En ocasiones la diarrea por rotavirus se debe a alteraciones de la absorción de sodio y glucosa a medida que las células lesionadas en las vellosidades son remplazadas por células inmaduras de las criptas que no absorben. El establecimiento de la función puede tardar tres a ocho semanas.
MANIFESTACIONES CLÍNICAS Y DIAGNÓSTICO DE LABORATORIO
Hay un periodo de incubación de uno a tres días. Los síntomas característicos consisten en diarrea liquida, fiebre, dolor abdominal y vomito, lo que desencadena deshidratación.
En los lactantes y en los niños, la perdida grave de electrolitos y líquidos puede ser mortal si no se trata. Los pacientes con casos más leves manifiestan síntomas durante tres a ocho días y luego se restablecen por completo. Sin embargo, la excreción viral en las heces puede persistir hasta por 50 días después de iniciada la diarrea. Se presentan infecciones asintomáticas, con seroconversión. En los niños con inmunodeficiencias, el rotavirus puede causar una enfermedad grave y prolongada.
El diagnostico de laboratorio se basa en la demostración del virus en las heces obtenidas en las primeras etapas de la enfermedad y en la elevación del título de anticuerpos. El virus en las heces se demuestra mediante enzimoinmunoanalisis (EIA) o microscopia inmunoelectronica (IEM). La prueba de EIA es más sensible que la de IEM. El método de detección mas sensible es la genotipificacion del acido nucleico del rotavirus obtenido de muestras de heces mediante reacción en cadena de la polimerasa. Se pueden utilizar las pruebas serológicas para detectar una elevación del título de anticuerpo, sobre todo ELISA.
TRATAMIENTO
El tratamiento de la gastroenteritis es sintomático, para corregir la perdida de agua y electrolitos que pueden desencadenar deshidratación, acidosis, choque y muerte del paciente. El tratamiento consiste en la reposición de líquidos y el restablecimiento del equilibrio electrolítico por vía intravenosa o por vía oral, como sea factible.
PARAMIXOVIRUS Y VIRUS DE LA RUBÉOLA
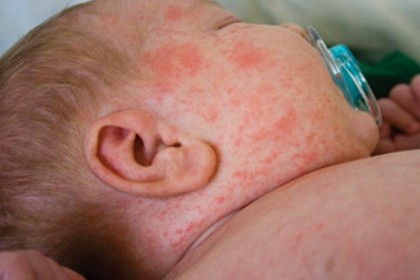
Los paramixovirus comprenden los microorganismos más importantes de las infecciones respiratorias de lactantes y niños pequeños (virus sincitial respiratorio y los virus de la parainfluenza), así como los microorganismos causantes de dos de las enfermedades contagiosas más frecuentes en la infancia (parotiditis y sarampión).
Todos los miembros de la familia Paramyxoviridae inician la infección a través del sistema respiratorio. La replicación de microorganismos patógenos respiratorios está limitada a los epitelios respiratorios, en tanto que el sarampión y la parotiditis se diseminan por todo el organismo y producen enfermedad generalizada.
El virus de la rubéola, aunque clasificado como un togavirus por sus propiedades químicas y físicas, puede considerarse dentro de los paramixovirus basándose en los aspectos epidemiológicos.
PROPIEDADES IMPORTANTES DE LOS PARAMIXOVIRUS
INFECCION POR EL VIRUS DEL SARAMPION
El sarampión es una enfermedad aguda muy contagiosa caracterizada por fiebre, síntomas respiratorios y un exantema maculo papuloso. Las complicaciones son frecuentes y pueden ser muy graves.
El ser humano es el único hospedador natural del virus del sarampión, aunque se pueden infectar en condiciones experimentales otras múltiples especies, como monos, perros y ratones. El virus logra acceso al cuerpo humano a través del sistema respiratorio, donde se multiplica en los tejidos locales; la infección se propaga luego al tejido linfoide regional donde ocurre una multiplicación adicional.
MANIFESTACIONES CLÍNICAS
Las infecciones en los hospedadores no inmunes casi siempre son sintomáticas. Tras un periodo de incubación de ocho a 12 días, el sarampión suele ser una enfermedad de siete a 11 días (con una fase prodrómica de dos a cuatro días seguida de una fase eruptiva de cinco a ocho días).
La fase prodrómica se caracteriza por fiebre, estornudos, tos, rinorrea, hiperemia conjuntival, manchas de Koplik y linfopenia. La tos y el coriza reflejan una reacción inflamatoria intensa que afecta a la mucosa del sistema respiratorio. La conjuntivitis suele acompañarse de fotofobia. Las manchas de Koplik (patognomónicas del sarampión) son pequeñas ulceraciones de color blanco azulado en la mucosa bucal opuesta a los molares inferiores. Estas manchas contienen células gigantes y antígenos virales y aparecen unos dos días después del exantema. La fiebre y la tos persisten hasta que el exantema aparece y luego desaparecen al cabo de uno a dos días.
El sarampión modificado ocurre en personas parcialmente inmunes, como los lactantes con anticuerpo materno residual. El periodo de incubación es prolongado, los síntomas prodrómicos están reducidos, las manchas de Koplik no suelen presentarse y el exantema es leve.
La complicación más frecuente del sarampión es la otitis media (5 a 9% de los casos). La neumonía es la complicación letal más frecuente del sarampión, causada por infecciones bacterianas secundarias. Las complicaciones que afectan al sistema nervioso central son las más graves. Alrededor del 50% de los niños con sarampión regular muestran cambios electroencefalográficos. La encefalitis aguda se presenta en casi 1:1 000 casos.
La panencefalitis esclerosante subaguda, la complicación tardía infrecuente de la infección por sarampión, tiene una incidencia de casi 1:300 000 casos. La enfermedad comienza de manera insidiosa cinco a 15 años después de un caso de sarampión; se caracteriza por deterioro mental progresivo, movimientos involuntarios, rigidez muscular y estado de coma. Suele ser mortal al cabo de uno a tres años después del inicio. Los pacientes con SSPE muestran cuantificaciones elevadas de anticuerpo del sarampión en el líquido cefalorraquídeo y virus del sarampión defectuoso en las células del cerebro. Con el empleo generalizado de la vacuna del sarampión, se ha vuelto menos frecuente la panencefalitis esclerosante subaguda.
DIAGNÓSTICO
El sarampión característico se diagnostica de manera fiable basándose en los datos clínicos; el diagnóstico de laboratorio puede ser necesario en los casos de sarampión modifi cados o atípicos.
Detección de antígeno y ácido nucleico. Los antígenos de sarampión pueden detectarse directamente en células epiteliales de secreciones respiratorias, la nasofaríngea, conjuntivas y orina. Los anticuerpos contra la nucleoproteína son útiles porque es la proteína viral más abundante en las células infectadas. La detección de RNA viral mediante RT-PCR es un método sensible que se puede aplicar a diversas muestras clínicas para el diagnóstico del sarampión.
Aislamiento e identificación del virus. Los frotis de secreciones nasofaríngeas y conjuntivales, las muestras de sangre, las secreciones respiratorias y la orina obtenidas de un paciente durante el periodo febril, son fuentes apropiadas para el aislamiento del virus. Las células de riñón de mono o persona o un linaje de células linfoblastoides (DP95-A), son óptimas para los intentos de aislamiento. El virus del sarampión crece con lentitud; los efectos citopáticos característicos (células gigantes multinucleadas que contienen cuerpos de inclusión intranuclear e intracitoplásmica) tardan siete a 10 días en desarrollarse.
Diagnóstico serológico. La confirmación serológica de la infección por el sarampión depende de un incremento de cuatro tantos en el título de anticuerpos entre los sueros de fase aguda y de fase convaleciente o de la demostración de anticuerpo de IgM específi co de sarampión en una sola muestra de suero obtenida entre una y dos semanas después del inicio del exantema. Las pruebas de ELISA se pueden utilizar para determinar anticuerpos del sarampión.
TRATAMIENTO
El tratamiento con vitamina A en los países en vías de desarrollo ha disminuido la mortalidad y la morbilidad. El virus del sarampión es susceptible in vitro a la inhibición por la ribavirina, pero no se han demostrado los beneficios clínicos.
INFECCIONES POR EL VIRUS DE LA RUBÉOLA
La rubéola es una enfermedad febril aguda que se caracteriza por un exantema y linfadenopatía que afecta a los niños y a los adultos jóvenes. Es el más leve de los exantemas virales frecuentes. Sin embargo, la infección durante las primeras etapas del embarazo puede producir anomalías importantes del feto, lo que comprende malformaciones congénitas y retraso mental. Las consecuencias de la rubéola in utero se designan como el síndrome de rubéola congénita.
CLASIFICACIÓN
El virus de la rubéola, un miembro de la familia Togaviridae, es el único miembro del género Rubivirus. Aunque sus características morfológicas y propiedades fisicoquímicas lo ubican en el grupo de los togavirus, la rubéola no es transmitida por artrópodos. Hay una diversidad de secuencia notable entre las cepas de virus de la rubéola. Actualmente se clasifican en dos grupos lejanamente relacionados y nueve genotipos.
SINDROME DE RUBEOLA CONGENITA
La viremia materna relacionada con la infección por rubéola durante el embarazo puede dar por resultado infección de la placenta y el feto. Sólo un número limitado de células fetales se infecta. La tasa de crecimiento de las células infectadas se reduce y esto da por resultado una menor cantidad de células en los órganos afectados al nacer. La infección puede desencadenar alteraciones e hipoplasia en el desarrollo de los órganos y desencadenar anomalías estructurales en el recién nacido.
MANIFESTACIONES CLÍNICAS
El virus de la rubéola se ha aislado en muchos órganos y tipos de células diferentes en lactantes infectados in utero y también la lesión provocada por la rubéola es difusa. Las manifestaciones clínicas del síndrome de rubéola congénita pueden agruparse en tres amplias categorías: 1) efectos transitorios en los lactantes, 2) manifestaciones permanentes que pueden ser ostensibles al nacer o que se reconocen durante el primer año y 3) anomalías del desarrollo que aparecen y evolucionan durante la infancia y la adolescencia.
La tríada característica de la rubéola congénita consiste en cataratas, anomalías cardiacas y sordera. Los lactantes también manifiestan síntomas transitorios de retraso del crecimiento, exantema, hepatoesplenomegalia, ictericia y meningoencefalitis. La infección del sistema nervioso central es más global. La manifestación del desarrollo más frecuente en la rubéola congénita es el retraso mental moderado a intenso. En los niños preescolares se presentan problemas de equilibrio y de las habilidades motoras. Los lactantes con afección grave pueden necesitar hospitalizarse.
La panencefalitis progresiva por la rubéola es una complicación nfrecuente que se presenta en el segundo decenio de vida en niños con rubéola congénita y consiste en un agravamiento neurológico que inevitablemente avanza al fallecimiento.
DIAGNÓSTICO
Aislamiento e identificación del virus. Detección de ácido nucleico. Diagnóstico serológico
TRATAMIENTO
No se dispone de ningún tratamiento específico para la rubéola congénita. Puede evitarse mediante la inmunización infantil con la vacuna de la rubéola para garantizar que las mujeres en edad de procrear sean inmunes.
Todos los miembros de la familia Paramyxoviridae inician la infección a través del sistema respiratorio. La replicación de microorganismos patógenos respiratorios está limitada a los epitelios respiratorios, en tanto que el sarampión y la parotiditis se diseminan por todo el organismo y producen enfermedad generalizada.
El virus de la rubéola, aunque clasificado como un togavirus por sus propiedades químicas y físicas, puede considerarse dentro de los paramixovirus basándose en los aspectos epidemiológicos.
PROPIEDADES IMPORTANTES DE LOS PARAMIXOVIRUS
- Virión: Esférico, polimorfo, 150 nm o más de diámetro (nucleocápside helicoidal, 13 a 18 nm)
- Genoma: RNA monocatenario, lineal, no segmentado, de polaridad negativa, no infeccioso
- Envoltura: Contiene la glucoproteína viral (G, H o HN) (que a veces es portadora de actividad de hemaglutinina o neuraminidasa) y glucoproteína de fusión (F); muy frágil
- Replicación: Citoplasma; las partículas experimentan gemación desde la membrana plasmática
- Características sobresalientes: Antigénicamente estable. Las partículas son lábiles pero muy infecciosas
INFECCION POR EL VIRUS DEL SARAMPION
El sarampión es una enfermedad aguda muy contagiosa caracterizada por fiebre, síntomas respiratorios y un exantema maculo papuloso. Las complicaciones son frecuentes y pueden ser muy graves.
El ser humano es el único hospedador natural del virus del sarampión, aunque se pueden infectar en condiciones experimentales otras múltiples especies, como monos, perros y ratones. El virus logra acceso al cuerpo humano a través del sistema respiratorio, donde se multiplica en los tejidos locales; la infección se propaga luego al tejido linfoide regional donde ocurre una multiplicación adicional.
MANIFESTACIONES CLÍNICAS
Las infecciones en los hospedadores no inmunes casi siempre son sintomáticas. Tras un periodo de incubación de ocho a 12 días, el sarampión suele ser una enfermedad de siete a 11 días (con una fase prodrómica de dos a cuatro días seguida de una fase eruptiva de cinco a ocho días).
La fase prodrómica se caracteriza por fiebre, estornudos, tos, rinorrea, hiperemia conjuntival, manchas de Koplik y linfopenia. La tos y el coriza reflejan una reacción inflamatoria intensa que afecta a la mucosa del sistema respiratorio. La conjuntivitis suele acompañarse de fotofobia. Las manchas de Koplik (patognomónicas del sarampión) son pequeñas ulceraciones de color blanco azulado en la mucosa bucal opuesta a los molares inferiores. Estas manchas contienen células gigantes y antígenos virales y aparecen unos dos días después del exantema. La fiebre y la tos persisten hasta que el exantema aparece y luego desaparecen al cabo de uno a dos días.
El sarampión modificado ocurre en personas parcialmente inmunes, como los lactantes con anticuerpo materno residual. El periodo de incubación es prolongado, los síntomas prodrómicos están reducidos, las manchas de Koplik no suelen presentarse y el exantema es leve.
La complicación más frecuente del sarampión es la otitis media (5 a 9% de los casos). La neumonía es la complicación letal más frecuente del sarampión, causada por infecciones bacterianas secundarias. Las complicaciones que afectan al sistema nervioso central son las más graves. Alrededor del 50% de los niños con sarampión regular muestran cambios electroencefalográficos. La encefalitis aguda se presenta en casi 1:1 000 casos.
La panencefalitis esclerosante subaguda, la complicación tardía infrecuente de la infección por sarampión, tiene una incidencia de casi 1:300 000 casos. La enfermedad comienza de manera insidiosa cinco a 15 años después de un caso de sarampión; se caracteriza por deterioro mental progresivo, movimientos involuntarios, rigidez muscular y estado de coma. Suele ser mortal al cabo de uno a tres años después del inicio. Los pacientes con SSPE muestran cuantificaciones elevadas de anticuerpo del sarampión en el líquido cefalorraquídeo y virus del sarampión defectuoso en las células del cerebro. Con el empleo generalizado de la vacuna del sarampión, se ha vuelto menos frecuente la panencefalitis esclerosante subaguda.
DIAGNÓSTICO
El sarampión característico se diagnostica de manera fiable basándose en los datos clínicos; el diagnóstico de laboratorio puede ser necesario en los casos de sarampión modifi cados o atípicos.
Detección de antígeno y ácido nucleico. Los antígenos de sarampión pueden detectarse directamente en células epiteliales de secreciones respiratorias, la nasofaríngea, conjuntivas y orina. Los anticuerpos contra la nucleoproteína son útiles porque es la proteína viral más abundante en las células infectadas. La detección de RNA viral mediante RT-PCR es un método sensible que se puede aplicar a diversas muestras clínicas para el diagnóstico del sarampión.
Aislamiento e identificación del virus. Los frotis de secreciones nasofaríngeas y conjuntivales, las muestras de sangre, las secreciones respiratorias y la orina obtenidas de un paciente durante el periodo febril, son fuentes apropiadas para el aislamiento del virus. Las células de riñón de mono o persona o un linaje de células linfoblastoides (DP95-A), son óptimas para los intentos de aislamiento. El virus del sarampión crece con lentitud; los efectos citopáticos característicos (células gigantes multinucleadas que contienen cuerpos de inclusión intranuclear e intracitoplásmica) tardan siete a 10 días en desarrollarse.
Diagnóstico serológico. La confirmación serológica de la infección por el sarampión depende de un incremento de cuatro tantos en el título de anticuerpos entre los sueros de fase aguda y de fase convaleciente o de la demostración de anticuerpo de IgM específi co de sarampión en una sola muestra de suero obtenida entre una y dos semanas después del inicio del exantema. Las pruebas de ELISA se pueden utilizar para determinar anticuerpos del sarampión.
TRATAMIENTO
El tratamiento con vitamina A en los países en vías de desarrollo ha disminuido la mortalidad y la morbilidad. El virus del sarampión es susceptible in vitro a la inhibición por la ribavirina, pero no se han demostrado los beneficios clínicos.
INFECCIONES POR EL VIRUS DE LA RUBÉOLA
La rubéola es una enfermedad febril aguda que se caracteriza por un exantema y linfadenopatía que afecta a los niños y a los adultos jóvenes. Es el más leve de los exantemas virales frecuentes. Sin embargo, la infección durante las primeras etapas del embarazo puede producir anomalías importantes del feto, lo que comprende malformaciones congénitas y retraso mental. Las consecuencias de la rubéola in utero se designan como el síndrome de rubéola congénita.
CLASIFICACIÓN
El virus de la rubéola, un miembro de la familia Togaviridae, es el único miembro del género Rubivirus. Aunque sus características morfológicas y propiedades fisicoquímicas lo ubican en el grupo de los togavirus, la rubéola no es transmitida por artrópodos. Hay una diversidad de secuencia notable entre las cepas de virus de la rubéola. Actualmente se clasifican en dos grupos lejanamente relacionados y nueve genotipos.
SINDROME DE RUBEOLA CONGENITA
La viremia materna relacionada con la infección por rubéola durante el embarazo puede dar por resultado infección de la placenta y el feto. Sólo un número limitado de células fetales se infecta. La tasa de crecimiento de las células infectadas se reduce y esto da por resultado una menor cantidad de células en los órganos afectados al nacer. La infección puede desencadenar alteraciones e hipoplasia en el desarrollo de los órganos y desencadenar anomalías estructurales en el recién nacido.
MANIFESTACIONES CLÍNICAS
El virus de la rubéola se ha aislado en muchos órganos y tipos de células diferentes en lactantes infectados in utero y también la lesión provocada por la rubéola es difusa. Las manifestaciones clínicas del síndrome de rubéola congénita pueden agruparse en tres amplias categorías: 1) efectos transitorios en los lactantes, 2) manifestaciones permanentes que pueden ser ostensibles al nacer o que se reconocen durante el primer año y 3) anomalías del desarrollo que aparecen y evolucionan durante la infancia y la adolescencia.
La tríada característica de la rubéola congénita consiste en cataratas, anomalías cardiacas y sordera. Los lactantes también manifiestan síntomas transitorios de retraso del crecimiento, exantema, hepatoesplenomegalia, ictericia y meningoencefalitis. La infección del sistema nervioso central es más global. La manifestación del desarrollo más frecuente en la rubéola congénita es el retraso mental moderado a intenso. En los niños preescolares se presentan problemas de equilibrio y de las habilidades motoras. Los lactantes con afección grave pueden necesitar hospitalizarse.
La panencefalitis progresiva por la rubéola es una complicación nfrecuente que se presenta en el segundo decenio de vida en niños con rubéola congénita y consiste en un agravamiento neurológico que inevitablemente avanza al fallecimiento.
DIAGNÓSTICO
Aislamiento e identificación del virus. Detección de ácido nucleico. Diagnóstico serológico
TRATAMIENTO
No se dispone de ningún tratamiento específico para la rubéola congénita. Puede evitarse mediante la inmunización infantil con la vacuna de la rubéola para garantizar que las mujeres en edad de procrear sean inmunes.
PAPILOMAVIRUS

EPIDEMIOLOGÍA
Las infecciones por HPV alcanzan su punto máximo en los adolescentes y jóvenes adultos menores de 25 años de edad.
El cáncer cervicouterino es el segundo cáncer más frecuente en las mujeres en todo el mundo (alrededor de 500 000 casos nuevos anuales) y constituye la causa principal de muerte por cáncer en los países subdesarrollados.
Con base en la frecuencia relativa de DNA viral en determinados cánceres, los tipos 16 y 18 de HPV se consideran de riesgo cancerígeno elevado.
Las infecciones virales se transmiten por contacto cercano. Las partículas virales se liberan de la superficie de las lesiones papilomatosas. Probablemente las microlesiones permiten la infección de las células de la capa basal proliferante en otros sitios o en distintos hospedadores.
Los papilomavirus infectan la piel y mucosas; provocan en ocasiones distintos tipos de verrugas como las cutáneas, plantares, planas, anogenitales, papilomas laríngeos y diversos cánceres, incluidos el cervicouterino, vulvar, del pene y anal y un subgrupo de cánceres de cabeza y cuello. Los múltiples tipos de cepas aisladas de HPV se vinculan con determinadas lesiones clínicas, aunque las pautas de distribución no son absolutas. Las infecciones genitales por HPV se transmiten por vía sexual y constituyen una de las enfermedades de transmisión sexual más frecuentes en Estados Unidos.
Algunos de los síntomas más importantes que sugieren la presencia de virus del papiloma humano son: Irritaciones constantes en la entrada de la vagina con ardor y sensación de quemadura durante las relaciones sexuales. Pequeñas verrugas en el área ano-genital: cérvix, vagina, vulva y uretra (en mujeres) y pene, uretra y escroto (en varones).
Pueden variar en apariencia (verrugas planas no visibles o acuminadas si visibles), número y tamaño.
DIAGNÓSTICO
Examen macroscópico: comprende la observación directa de las verrugas genitales; se puede utilizar ácido acético, que tiñe de blanco las lesiones. Así mismo, se observa mediante colposcopia del cuello uterino y la vagina, previamente teñida con yodo o ácido acético.
Examen microscópico: observación de células sospechosas con cambios coilocíticos en citologías de cuello uterino y vagina en mujeres, usando la tinción de Papanicolaou. Se pueden tomar biopsias de lesiones sospechosas, o incluso de vegetaciones o verrugas genitales, tanto de hombres como de mujeres, y enviar las muestras a una sección de anatomía patológica para su análisis.
Detección directa del material genético del virus por técnicas de biología molecular, que amplifican el ADN del virus y permiten la identificación de los distintos serotipos.
TRATAMINETO
Actualmente no hay tratamiento médico para las infecciones por VPH. Sin embargo, las verrugas genitales y las lesiones precancerosas que resultan de las infecciones por VPH pueden tratarse.
Los métodos que se usan comúnmente para tratar las lesiones precancerosas cervicales son la criocirugía (congelación para destruir los tejidos); el procedimiento de escisión electroquirúrgica con asa, o la extirpación de tejido del cérvix o cuello uterino mediante una asa de alambre caliente.
Los tratamientos para otros tipos de lesiones precancerosas causadas por VPH (lesiones de vagina, de pene y de ano) y las verrugas genitales son los productos químicos tópicos o fármacos, la cirugía por escisión, la criocirugía, la electrocirugía y la cirugía con láser.
Las infecciones por HPV alcanzan su punto máximo en los adolescentes y jóvenes adultos menores de 25 años de edad.
El cáncer cervicouterino es el segundo cáncer más frecuente en las mujeres en todo el mundo (alrededor de 500 000 casos nuevos anuales) y constituye la causa principal de muerte por cáncer en los países subdesarrollados.
Con base en la frecuencia relativa de DNA viral en determinados cánceres, los tipos 16 y 18 de HPV se consideran de riesgo cancerígeno elevado.
- Virión: Icosaédrico, 55 nm de diámetro
- Genoma: DNA bicatenario, circular, 8 kbp, PM 5 millones
- Proteínas: Dos proteínas estructurales; las histonas celulares condensan DNA en el virión
- Cubierta: Ninguna
- Replicación: Núcleo
- Características principales: Estimula la síntesis de DNA celular. Gama de hospedadores y tropismo hístico limitado. Causa importante de cáncer en el humano, especialmente cervicouterino. Las oncoproteínas virales interactúan con las proteínas supresoras de tumores celulares
Las infecciones virales se transmiten por contacto cercano. Las partículas virales se liberan de la superficie de las lesiones papilomatosas. Probablemente las microlesiones permiten la infección de las células de la capa basal proliferante en otros sitios o en distintos hospedadores.
Los papilomavirus infectan la piel y mucosas; provocan en ocasiones distintos tipos de verrugas como las cutáneas, plantares, planas, anogenitales, papilomas laríngeos y diversos cánceres, incluidos el cervicouterino, vulvar, del pene y anal y un subgrupo de cánceres de cabeza y cuello. Los múltiples tipos de cepas aisladas de HPV se vinculan con determinadas lesiones clínicas, aunque las pautas de distribución no son absolutas. Las infecciones genitales por HPV se transmiten por vía sexual y constituyen una de las enfermedades de transmisión sexual más frecuentes en Estados Unidos.
Algunos de los síntomas más importantes que sugieren la presencia de virus del papiloma humano son: Irritaciones constantes en la entrada de la vagina con ardor y sensación de quemadura durante las relaciones sexuales. Pequeñas verrugas en el área ano-genital: cérvix, vagina, vulva y uretra (en mujeres) y pene, uretra y escroto (en varones).
Pueden variar en apariencia (verrugas planas no visibles o acuminadas si visibles), número y tamaño.
DIAGNÓSTICO
Examen macroscópico: comprende la observación directa de las verrugas genitales; se puede utilizar ácido acético, que tiñe de blanco las lesiones. Así mismo, se observa mediante colposcopia del cuello uterino y la vagina, previamente teñida con yodo o ácido acético.
Examen microscópico: observación de células sospechosas con cambios coilocíticos en citologías de cuello uterino y vagina en mujeres, usando la tinción de Papanicolaou. Se pueden tomar biopsias de lesiones sospechosas, o incluso de vegetaciones o verrugas genitales, tanto de hombres como de mujeres, y enviar las muestras a una sección de anatomía patológica para su análisis.
Detección directa del material genético del virus por técnicas de biología molecular, que amplifican el ADN del virus y permiten la identificación de los distintos serotipos.
TRATAMINETO
Actualmente no hay tratamiento médico para las infecciones por VPH. Sin embargo, las verrugas genitales y las lesiones precancerosas que resultan de las infecciones por VPH pueden tratarse.
Los métodos que se usan comúnmente para tratar las lesiones precancerosas cervicales son la criocirugía (congelación para destruir los tejidos); el procedimiento de escisión electroquirúrgica con asa, o la extirpación de tejido del cérvix o cuello uterino mediante una asa de alambre caliente.
Los tratamientos para otros tipos de lesiones precancerosas causadas por VPH (lesiones de vagina, de pene y de ano) y las verrugas genitales son los productos químicos tópicos o fármacos, la cirugía por escisión, la criocirugía, la electrocirugía y la cirugía con láser.